

| A. | X分子中有2个手性碳原子 | |
| B. | Y分子中所有原子可能在同一平面内 | |
| C. | 可用FeCl3溶液或NaHCO3溶液鉴别X和Y | |
| D. | 在NaOH溶液中,1molM最多可与5molNaOH发生反应 |
分析 A.连接4个不同原子或原子团的碳原子为手性碳原子;
B.碳碳双键与碳氧双键为平面结构,旋转碳碳单键可以3个平面处于同一平面,旋转C-O单键可以使H原子处于平面内;
C.X含有酚羟基,可以与氯化铁溶液发生显色反应,而Y没有酚羟基,但Y含有羧基,能与碳酸氢钠反应生成二氧化碳,而X中酚羟基不能与碳酸氢钠反应;
D.酚羟基、酯基、肽键均与氢氧化钠反应,结构中酯基为羧酸与酚形成的酯基,1mol该酯基能与2molNaOH反应.
解答 解:A.X中只有连接氨基的碳原子连接4个不同原子团的碳原子为手性碳原子,故A错误;
B.碳碳双键与碳氧双键为平面结构,旋转碳碳单键可以3个平面处于同一平面,旋转C-O单键可以使H原子处于平面内,Y分子中所有原子可能在同一平面内,故B正确;
C.X含有酚羟基,可以与氯化铁溶液发生显色反应,而Y没有酚羟基,可以用FeCl3溶液鉴别,Y含有羧基,能与碳酸氢钠反应生成二氧化碳,而X中酚羟基不能与碳酸氢钠反应,也可以用NaHCO3溶液鉴别,故C正确;
D.酚羟基、酯基、肽键均与氢氧化钠反应,结构中酯基为羧酸与酚形成的酯基,1mol该酯基能与2molNaOH反应,1molM能与6molNaOH反应,故D错误,
故选:BC.
点评 本题考查有机物结构与性质,B选项需要学生具备一定的空间想象,注意通过旋转单键判断共面可能性,C为易错点,学生容易忽略题目中酯基与氢氧化钠反应比例关系.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:解答题
| 实 验 步 骤 | 实 验 结 论 |
| (1)将9.0g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过足量的浓硫酸和碱石灰,发现两者分别增重5.4g和13.2g. | (1)A的实验式为CH2O. |
| (2)通过质谱法测得其相对分子质量为90. | (2)A的分子式为C3H6O3. |
| (3)另取9.0g A,跟足量的NaHCO3粉末反应,生成2.24L CO2(标准状况),若与足量金属钠反应则生成2.24L H2(标准状况). | (3)A中含有的官能团名称为羧基、羟基. |
| (4)A的核磁共振氢谱有四组吸收峰,其峰面积之比为2:2:1:1. | (4)综上所述,A的结构简式为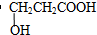 . .(5)写出A与NaHCO3反应的化学方程式 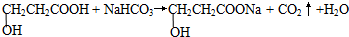 . . |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 试管内壁附着的硫黄可以用热的KOH溶液洗涤,也可以用CS2洗涤 | |
| B. | 盛Na2SO3、Na2S溶液的试剂瓶不能用玻璃塞,贮存时应盖好瓶塞,防止被空气氧化 | |
| C. | 金属镁着火可使用扑救金属火灾的专用干粉灭火剂灭火,但不可用泡沫灭火器灭火 | |
| D. | 从硫酸亚铁铵溶液中获取硫酸亚铁铵晶体,可以用蒸发结晶,也可以用冷却结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
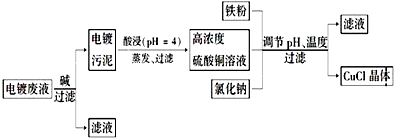
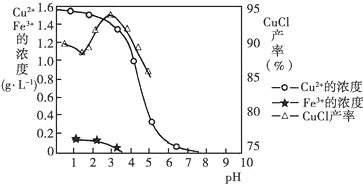
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、SO42-、Cl-、NO3- | B. | Na+、HCO3-、Ca2+、Cl- | ||
| C. | Na+、Cl-、NO3-、Fe3+ | D. | K+、Cl、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Na+、NO3-、CO32- | B. | H+、Na+、ClO-、Cl- | ||
| C. | K+、HCO3-、Cl-、OH- | D. | Na+、Mg2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用外接直流电源保护铁质建筑物,属于电化学中牺牲阳极的阴极保护法 | |
| B. | 科学仪器的使用利于我们认识物质的微观世界,现在人们借助扫描隧道显微镜,应用SMT技术可以“看”到越来越细微的结构,并实现对原子或分子的操纵 | |
| C. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大 | |
| D. | 汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,加快该反应的速率,同时能提高该反应的平衡转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com