
【题目】含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6ClF3=6CoF3+3Cl2+4X。下列有关该反应的说法,正确的是( )
A.X与O3互为同位素
B.1 mol Co3O4在反应中转移9 mol电子
C.ClF3中氯元素为-3价
D.Co3O4在反应中作氧化剂
【答案】B
【解析】
含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6ClF3=6CoF3+3Cl2+4X,根据质量守恒,X为O2,Co3O4在反应中O元素的化合价由-2价升高为0价,Co的化合价由+![]() 升高到+3价,被氧化,Co3O4作还原剂,ClF3在反应中Cl元素的化合价由+3价降低为0价,被还原,CClF3作氧化剂,据此分析解答。
升高到+3价,被氧化,Co3O4作还原剂,ClF3在反应中Cl元素的化合价由+3价降低为0价,被还原,CClF3作氧化剂,据此分析解答。
A.X为O2,与O3互为同素异形体,故A错误;
B.Co3O4在反应中O元素的化合价由-2价升高为0价,Co的化合价由+![]() 升高到+3价,lmol Co3O4参加反应转移的电子为[2×4+3×(3-
升高到+3价,lmol Co3O4参加反应转移的电子为[2×4+3×(3-![]() )]mol=9 mol电子,故B正确;
)]mol=9 mol电子,故B正确;
C.ClF3中氯元素为+3价,故C错误;
D.Co3O4在反应中O元素的化合价由-2价升高为0价,Co的化合价由+![]() 升高到+3价,被氧化,Co3O4作还原剂,故D错误。
升高到+3价,被氧化,Co3O4作还原剂,故D错误。
故选B。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】液体锌二次电池具有电压高、成本低、安全性强和可循环使用等特点。已知:①Zn(OH)2+2OH-=Zn(OH)![]() ;②KOH凝胶中允许离子存在、生成或迁移。下列说法错误的是
;②KOH凝胶中允许离子存在、生成或迁移。下列说法错误的是
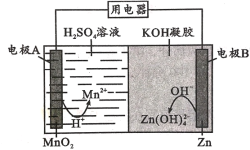
A.电池放电时,电子由电极B经导线流向电极A
B.电池反应为MnO2+ Zn + 4H++4OH-=Mn2+ + Zn(OH)![]() +2 H2 O
+2 H2 O
C.电池充电时,H+向电极A移动
D.电池充电时,电极B的质量增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 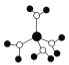 水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
B. 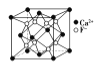 CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
C.  H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
D.  金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解合成 1 , 2-二氯乙烷的实验装置如图所示。下列说法中正确的是
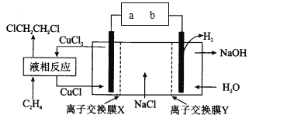
A.a为电源的负极
B.CuCl2能将C2H4还原为 l , 2-二氯乙烷
C.X、Y依次为阳离子交换膜、阴离子交换膜
D.该装置总反应为CH2=CH2+ 2H2O + 2NaCl![]() H2+ 2NaOH + ClCH2CH2Cl
H2+ 2NaOH + ClCH2CH2Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿水青山就是金山银山”,研究NOx、SO2等大气污染物的妥善处理具有重要意义。
CO 还原NO 的脱硝反应:2CO(g)+2NO(g) 2CO2(g)+N2(g) △H
(1)已知:CO(g)+NO2(g) CO2(g)+NO(g) △H1=-226 kJ·mol-1
N2(g)+2O2(g) 2NO2(g) △H2=+68 kJ·mol-1
N2(g)+O2(g) 2NO(g) △H3=+183 kJ·mol-1
脱硝反应△H=__________,有利于提高NO 平衡转化率的条件是________________(写出两条)。
(2)燃煤发电厂常利用反应2CaCO3(s)+2SO2(g)+O2(g) ![]() 2CaSO4(s)+2CO2(g) ΔH=-681.8kJ·mol-1,对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
2CaSO4(s)+2CO2(g) ΔH=-681.8kJ·mol-1,对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
时间/min 浓度/mol·L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
O2 | 1.00 | 0.79 | 0.60 | 0.60 | 0.64 | 0.64 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 0.88 | 0.88 |
①0~10min内,平均反应速率v(CO2)=___mol·L-1·min-1。
②30min后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是________(填字母)。
A.加入一定量的粉状碳酸钙
B.适当缩小容器的体积
C.通入一定量的O2
D.加入合适的催化剂
(3)NOx的排放主要来自于汽车尾气。
有人利用反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH= -34.0kJ·mol-1,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH= -34.0kJ·mol-1,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
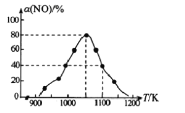
由图可知,1050K前反应中NO的转化率随温度升髙而增大,其原因为______________。
(4)为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH=-746.8kJ·mol-1,生成无毒的N2和CO2实验测得,v正=k正c2(NO)·c2(CO),v逆=k逆c(N2) c2(CO2)(k正、k逆为速率常数,只与温度有关)。
N2(g)+2CO2(g) ΔH=-746.8kJ·mol-1,生成无毒的N2和CO2实验测得,v正=k正c2(NO)·c2(CO),v逆=k逆c(N2) c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅降低温度,k正减小的倍数________(填“>”、“<”或“=”)k逆减小的倍数。
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为20%,则![]() =________(计算结果用分数表示)
=________(计算结果用分数表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在pH=1的某溶液中可能有Na+、Fe3+、Fe2+、I-、Cl- 、![]() 中的几种,现取100mL该溶液进行如下实验。根据实验结果,下列判断正确的是
中的几种,现取100mL该溶液进行如下实验。根据实验结果,下列判断正确的是

A.Fe2+、I-、Cl-三种离子一定存在
B.![]() 一定不存在,不能确定Na+和Cl-是否存在
一定不存在,不能确定Na+和Cl-是否存在
C.Fe3+与Fe2+至少有一种
D.该溶液中c(Cl-)至少为0.2molL1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种有机物分子中的碳原子数目相同,标准状况下烃A对氢气的相对密度是13;烃B跟HBr反应生成C;C与D混合后加入NaOH并加热,可生成B。
(1)写出有机物的结构简式:A____;B_____C______;D__________
(2)写出有关反应的化学方程式:____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A、B均为合成某种抗支气管哮喘药物的中间体,A在一定条件下可转化为B(如图所示),下列说法正确的是
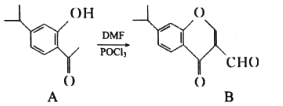
A.分子A中至少有8个碳原子位于同一平面
B.![]() 与浓溴水发生取代反应时,最多消耗
与浓溴水发生取代反应时,最多消耗![]()
C.物质B能发生银镜反应,也能发生水解反应
D.![]() 最多可与
最多可与![]() 发生加成反应
发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)键线式![]() 表示的分子式为_________,名称是____________。
表示的分子式为_________,名称是____________。
(2)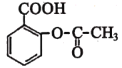 含有的官能团的名称为_____________,写出该物质在酸性环境下水解产物的结构简式__________、__________。
含有的官能团的名称为_____________,写出该物质在酸性环境下水解产物的结构简式__________、__________。
(3)甲醇在铜作催化剂加热时与氧气反应的化学方程式为_________________。
(4)某烷烃B 的结构简式为CH3CH(CH3)CH(C2H5)2, 有一种烷烃C与烷烃B是同分异构体,它却不能由任何烯烃催化加氢得到,则C的结构简式为____________。
(5)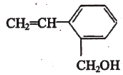 最多______个原子共平面,写出该物质发生加聚反应的化学方程式_________。
最多______个原子共平面,写出该物质发生加聚反应的化学方程式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com