
【题目】液体锌二次电池具有电压高、成本低、安全性强和可循环使用等特点。已知:①Zn(OH)2+2OH-=Zn(OH)![]() ;②KOH凝胶中允许离子存在、生成或迁移。下列说法错误的是
;②KOH凝胶中允许离子存在、生成或迁移。下列说法错误的是
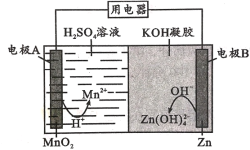
A.电池放电时,电子由电极B经导线流向电极A
B.电池反应为MnO2+ Zn + 4H++4OH-=Mn2+ + Zn(OH)![]() +2 H2 O
+2 H2 O
C.电池充电时,H+向电极A移动
D.电池充电时,电极B的质量增大
【答案】C
【解析】
由图中信息可知,电极A上发生还原反应,电极B上发生氧化反应,则A为正极、B为负极。
A. 电池放电时,电子由负极经外电路流向正极,即由电极B经导线流向电极A,A说法正确;
B. 由图中两电极的物质转化关系可知,电池反应为MnO2+ Zn + 4H++4OH-=Mn2+ + Zn(OH)![]() +2 H2 O,B说法正确;
+2 H2 O,B说法正确;
C. 电池放电时,K+向正极迁移,即向电极A迁移;电池充电时,电极A变为阳极,电极反应式为Mn2+ +2 H2 O -2e- = MnO2+ 4H+;电极B变为阴极,电极反应式为Zn(OH)![]() + 2e+= Zn +4OH-,K+向阴极迁移,即向电极B移动,H+不可能向电极A移动,C说法错误;
+ 2e+= Zn +4OH-,K+向阴极迁移,即向电极B移动,H+不可能向电极A移动,C说法错误;
D. 电池充电时,电极B变为阴极,电极反应式为Zn(OH)![]() + 2e+= Zn +4OH-,电极B的质量增大,D说法正确。
+ 2e+= Zn +4OH-,电极B的质量增大,D说法正确。
本题选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知有下列三种有机物:
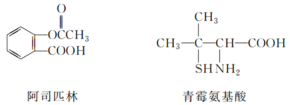
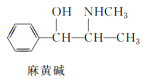
下列叙述不正确的是( )
A.三种有机物都能发生取代反应
B.1mol阿司匹林最多能与3molNaOH反应
C.麻黄碱属于芳香烃,苯环上的一氯代物有3种
D.青霉氨基酸既能与盐酸反应,又能与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,在水中存在沉淀溶解平衡:CdS(s)![]() Cd2+(aq)+S2-(aq),其溶度积Ksp=c(Cd2+)·c(S2-),其在水中的沉淀溶解平衡曲线如图所示(T2>T1)。下列说法错误的是( )
Cd2+(aq)+S2-(aq),其溶度积Ksp=c(Cd2+)·c(S2-),其在水中的沉淀溶解平衡曲线如图所示(T2>T1)。下列说法错误的是( )
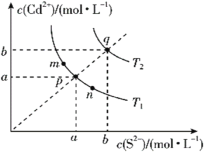
A.T1时CdS在c(S2-)=0.01mol/L的Na2S溶液中,c(Cd2+)=100a2mol/L
B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀是应用电解原理在某些金属表面镀上一薄层其它金属或合金的方法。在铁质铆钉上镀镍(Ni)能防止铁被腐蚀,如图1。实验室模拟铁片镀镍,装置如图2。

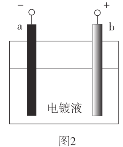
(1)b极材料是__。
(2)电镀液中含有NiSO4、NaCl和硼酸。
已知:NiSO4=Ni2++SO![]() 、Ni2++2H2ONi(OH)2+2H+
、Ni2++2H2ONi(OH)2+2H+
①a极的电极反应式是__。
②硼酸的作用是调节溶液的pH。pH较小时,a极易产生__气体,使镀层疏松多孔。pH较大时,a极会吸附__固体而使镀层含有杂质。
(3)铁质铆钉上镀镍能防止铁被腐蚀是因为镀层使铁与__等物质隔离。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.升高H2SO4稀溶液温度,溶液中c(OH-)增大
B.pH=3的CH3COOH溶液加入CH3COONa固体,溶液的pH减小
C.NaClO稀溶液中加入NaClO固体,溶液中![]() 增大
增大
D.向AgCl、Ag2CrO4的饱和溶液中加入少量AgNO3固体,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,资源化利用CO2具有重要的工业与环境意义。
(1)下列物质理论上可以作为CO2捕获剂的是____(填序号)。
A.NH4Cl溶液 B.(NH4)2CO3溶液 C.氨水 D.稀H2SO4
(2)以TiO2为催化剂的光热化学循环分解CO2反应为碳减排提供了一个新途径。该反应的机理及各分子化学键完全断裂时的能量变化如下图所示。
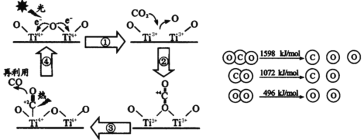
该转化过程①中会____能量(填“吸收”或“释放”);CO2分解反应的热化学方程式为______,实现该反应的能量转化方式是________。
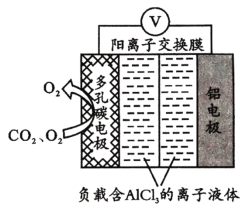
(3)O2辅助的Al-CO2电池能有效利用CO2,且电池反应产物Al2(C2O4)。是重要的化工原料,工作原理如图所示。若正极上CO2还原生成C2O![]() ,则正极的反应式为___;电路中转移1 mol电子,需消耗CO2_____L(标准状况)。
,则正极的反应式为___;电路中转移1 mol电子,需消耗CO2_____L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A.24g镁与27g铝中,质子数之比为12∶13
B.相同质量的16O2和18O2,体积比为9∶8
C.将1LCmol·L-1氯化钠溶液加入水中稀释为5L,得到0.2Cmol·L-1氯化钠溶液
D.同温同压时,H2和CH4两种气体的密度之比为1∶8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铬(Cr)在自然界主要以+3价和+6价存在。请回答下列问题:
(1)利用铬铁矿(FeO·Cr2O3)冶炼制取金属铬的工艺流程如图所示:
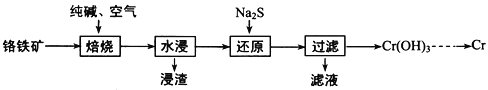
①为加快焙烧速率和提高原料的利用率,可采取的措施之一是_________。
②“水浸”要获得浸出液的操作是________。
(2)常温下,已知Cr3+完全沉淀时溶液pH为5,(Cr3+浓度降至10-5mol·L-1可认为完全沉淀)则Cr(OH)3的溶度积常数Ksp=___。
(3)用石墨电极电解铬酸钠(Na2CrO4)溶液,可制重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2![]() +2H+2
+2H+2![]() +2H2O)
+2H2O)
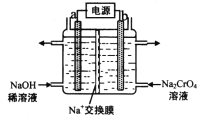
①电极b连接电源的______极(填“正”或“负),b极发生的电极反应:________
②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则理论上生成重铬酸钠的物质的量是________mol(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6ClF3=6CoF3+3Cl2+4X。下列有关该反应的说法,正确的是( )
A.X与O3互为同位素
B.1 mol Co3O4在反应中转移9 mol电子
C.ClF3中氯元素为-3价
D.Co3O4在反应中作氧化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com