
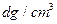 ,其摩尔质量为
,其摩尔质量为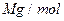 ,则该晶胞的体积是 。(请列出算式)
,则该晶胞的体积是 。(请列出算式)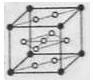
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
| | | | | |
| A | | D | | |
| | | E | G | M |
 (3)E、G元素的原子均可形成与M原子电子层结构相同的简单离子,且E离子的半径更大,请解释 。
(3)E、G元素的原子均可形成与M原子电子层结构相同的简单离子,且E离子的半径更大,请解释 。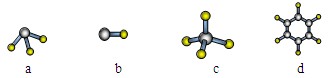
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 图是 ,第一电离能最小的元素的原子轨道表达式_______________________。
图是 ,第一电离能最小的元素的原子轨道表达式_______________________。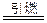 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平) _________________
_________________查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a=b-1 | B.a=b-11 | C.b="a+25"  | D.b=a+30 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
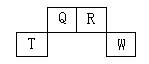
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
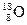 、②
、②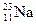 、③
、③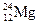 、④
、④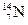 。用①、②、③、④回答:
。用①、②、③、④回答: 微粒中质子数小于中子数的是 ,
微粒中质子数小于中子数的是 ,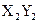 型化合物的是 。
型化合物的是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com