
【题目】已知:还原性强弱:I- >Fe2+。往100 mL碘化亚铁溶液中缓慢通入3.36 L(标准状况)氯气,反应完成后溶液中有1/2的Fe2+被氧化成Fe3+。则原碘化亚铁溶液的物质的量浓度为
A. 1.1mol·L-1 B. 1.5mol·L-1 C. 1.2mol·L-1 D. 1.0mol·L-1
【答案】C
【解析】
本题学生首先要明确:氧化还原反应中还原性强的离子先反应。并抓住氧化还原反应的实质:电子的转移,最后明确计算技巧:电子得失相等。
发生反应:①Cl2+ 2I-= 2Cl-+ I2
②Cl2+ 2Fe2+= 2Cl-+ 2Fe3+
设:原溶液的物质的量浓度为:C mol/L
碘化亚铁FeI2共为:0.1C mol
碘离子共:0.1C×2 =" 0.2C" mol
亚铁离子共为:0.1C mol 反应一半则为:0.1C×![]() =" 0.05C" mol
=" 0.05C" mol
失去电子共为:0.2C×1+0.05C×1 =" 0.25C" mol
氯气共:![]() =" 0.15" mol 则得到电子共:0.15×2 =" 0.3" mol
=" 0.15" mol 则得到电子共:0.15×2 =" 0.3" mol
得失电子相等:0.3 = 0.25C 解得:C =" 1.2" mol/L
所以:选C


科目:高中化学 来源: 题型:
【题目】用18mol/L浓硫酸配制100 mL 3.0mol/L稀硫酸的实验步骤如下:①计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③溶解;④转移、洗涤;⑤定容、摇匀。回答下列问题:
(1)所需浓硫酸的体积是_________,(保留一位小数)量取浓硫酸所用的量筒的规格是________ 。(从下列中选用 A. 10mL B. 25mL C. 50mL D. 100mL)
(2)第③步实验的操作是________________________________________。
(3)第⑤步实验的操作是______________________________。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中________;B.容量瓶用蒸馏水洗涤后残留有少量的水________;C.所用过的烧杯、玻璃棒未洗涤________;D.定容时俯视溶液的凹液面________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源标准的有( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②⑤⑥⑦B.⑤⑥⑦⑧
C.③⑤⑥⑦⑧D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某有机物A的结构,做如下实验:

①将4.4g该有机物完全燃烧,生成 0.2mol CO2和3.6g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③A的核磁共振氢谱如图2:
试回答下列问题:
(1)有机物A的相对分子质量是_____________
(2)有机物A的实验式是_____________
(3)有机物A的分子式是_____________
(4)红外光谱上发现A有﹣COOH和2个﹣CH3则有机物A的结构简式 ________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C,在周期表中所处的位置如图所示。A、B、C三种元素原子质子数之和为32。D元素原子的最外层电子数为其次外层电子数的2倍。则下列说法正确的是

A. 元素D形成的气态氢化物一定是正四面体型分子
B. B、C两种元素可形成BC6型化合物,该化合物在空气中能燃烧
C. 四种元素形成的气态氢化物中,C元素形成的氢化物的稳定性最大
D. A、B两种元素的气态氢化物均能与它们对应的最高价氧化物对应的水化物发生反应,且反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业碳酸钠纯度约为98%中含有Mg2+、Fe2+、Cl-和SO42-等杂质,提纯工艺流程如下:
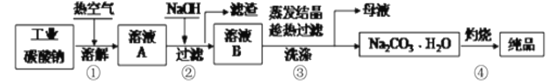
下列说法不正确的是
A. 步骤①,通入热空气可加快溶解速率
B. 步骤②,产生滤渣的离子反应为:![]()
C. 步骤③,趁热过滤时温度控制不当会使![]() 中混有
中混有![]() 等杂质
等杂质
D. 步骤④,灼烧时用到的主要仪器有铁坩埚、泥三角、三脚架、酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常状况下,CO是一种无色、无味、有毒的气体,难溶于水,与酸、碱、盐溶液均不反应。酒精喷灯可用作高温热源。正确连接如图所示的装置进行实验,可以验证某混合气体的成分是CO2和CO(每套装置限用一次)。请回答下列问题:
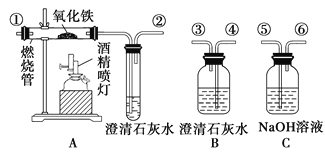
(1)连接装置导管口的顺序:混合气体→__________________→尾气处理(填导管接口代号)。
(2)证明原混合气体中CO2存在的实验现象是__________________________________;
证明CO存在的有关反应的化学方程式是__________________________________________。
(3)有同学提出仪器B应再使用一次,你认为有道理吗?________(填“有”或“没有”),并简述理由:
_________________________________________________________________。
(4)本实验尾气处理的方法是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A 萃取分液法 B 结晶法 C 分液法 D 蒸馏法 E 过滤法 F 渗析法
①_____分离饱和食盐水与沙子的混合物。
②_____分离水和汽油的混合物。
③_____分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物。
④_____从碘的水溶液里提取碘。
⑤_____从硝酸钾和氯化钠的混合液中获得硝酸钾。
Ⅱ.下图是某同学设计的蒸馏装置图
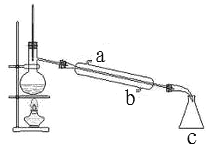
①进水口是_____(a 或 b)。
②装置 c 的名称是_____。
③蒸馏烧瓶中常加入沸石或碎瓷片,其目的是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素在元素周期表中的位置,取决于元素原子的( )
A.相对原子质量和核电荷数B.电子层数和中子数
C.电子层数和最外层电子数D.电子层数和核外电子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com