
【题目】用18mol/L浓硫酸配制100 mL 3.0mol/L稀硫酸的实验步骤如下:①计算所用浓硫酸的体积;②量取一定体积的浓硫酸;③溶解;④转移、洗涤;⑤定容、摇匀。回答下列问题:
(1)所需浓硫酸的体积是_________,(保留一位小数)量取浓硫酸所用的量筒的规格是________ 。(从下列中选用 A. 10mL B. 25mL C. 50mL D. 100mL)
(2)第③步实验的操作是________________________________________。
(3)第⑤步实验的操作是______________________________。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中________;B.容量瓶用蒸馏水洗涤后残留有少量的水________;C.所用过的烧杯、玻璃棒未洗涤________;D.定容时俯视溶液的凹液面________;
【答案】16.7mL B 先向烧杯加入少量蒸馏水,然后将浓硫酸沿烧杯内壁缓慢倒入烧杯中,并用玻璃棒搅拌 继续向容量瓶注入蒸馏水至离刻度线1-2cm处,改出胶头滴管向容量瓶滴加至凹液面与刻度线相切为止。塞紧瓶塞,倒转摇匀 偏小 无影响 偏小 偏大
【解析】
(1)稀释前后溶质的物质的量保持不变,即c浓×V浓= c稀×V稀,且量筒的精确度一般为0.1 mL,则V浓=![]() =16.7 mL;根据大而近原则,因此应选择25 mL量筒;故答案为:16.7mL、B;
=16.7 mL;根据大而近原则,因此应选择25 mL量筒;故答案为:16.7mL、B;
(2)浓硫酸溶解于水时放热,为了防止暴沸引起安全事故,稀释浓硫酸时,应该先向烧杯中加入适量水,再沿烧杯内壁缓缓加入浓硫酸,边加入边用玻璃棒搅拌,使之充分散热;故答案为:先向烧杯加入少量蒸馏水,然后将浓硫酸沿烧杯内壁缓慢倒入烧杯中,并用玻璃棒搅拌;
(3)定容:当液面在刻度线下1~2cm时,改用胶头滴管加蒸馏水至刻度线与凹液面相切;摇匀:盖好瓶塞,反复上下颠倒;故答案为:继续向容量瓶注入蒸馏水至离刻度线1-2cm处,改出胶头滴管向容量瓶滴加至凹液面与刻度线相切为止,塞紧瓶塞,倒转摇匀;
(4)A.浓硫酸具有吸水性,长时间放置在密封不好的容器中,会逐渐变稀,该情况能使所量取16.7mL液体所含硫酸的物质的量偏小,结果偏小;
B.容量瓶用蒸馏水洗涤后残留有少量的水,对溶质的量和溶液的体积无影响,故对溶液的浓度无影响;
C.所用过的烧杯、玻璃棒未洗涤导致溶质损失,所配溶液的浓度偏小;
D.定容时俯视溶液的凹液面会造成溶液的体积偏小,溶液的浓度偏大;
故答案为:偏小、无影响、偏小、偏大。


科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. Cu和NaOH溶液均能导电,故Cu和NaOH均为电解质
B. 水溶液中,1 mol KCl比1 mol KClO3电离出的Cl-多
C. NH3溶于水后,溶液能够导电,但NH3是非电解质
D. NaHSO4溶于水电离方程式为NaHSO4===Na++H++SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 某原子的摩尔质量是Mgmol-1,则一个该原子的真实质量为![]() g
g
B. 氢氧化钠的摩尔质量为40g
C. 1 mol氧原子的质量就是氧的相对原子质量
D. H2SO4的摩尔质量为96g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3X(g)+Y(g) ![]() Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
(1)升高温度:____________;
(2)增大压强:____________;
(3)增大容器容积:______________;
(4)加入X:______________;
(5)加入Y:______________;
(6)压缩体积:______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在27.50g水中溶解12.50g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.21g/cm3,该溶液中CuSO4的物质的量_________,该溶液中阴阳离子的总物质的量__________,该溶液中CuSO4的物质的量浓度_________,取出20.00 mL该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是 _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于平衡常数的说法正确的是
A. 在平衡常数表达式中,反应物浓度用起始浓度表示,生成物浓度用平衡浓度表示
B. 可逆反应中,反应物的转化率增大,一定导致化学平衡常数增大
C. 可以用化学平衡常数来定量描述化学反应的限度
D. 平衡常数的大小与温度、浓度、压强、催化剂有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中,不正确的是( )

A. 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
B. 试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
C. 实验时加热试管a的目的是加快反应速率并及时将乙酸乙酯蒸出
D. 试管b中饱和Na2CO3溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)被称为第三代半导体材料,其应用已经取得了突破性的进展。
已知:(i)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱。
(ii)NiCl2 溶液在加热时,先转化为Ni(OH)2,后分解为NiO。
(iii)制备氮化镓的反应为:2Ga+2NH3![]() 2GaN+3H2
2GaN+3H2
某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示:
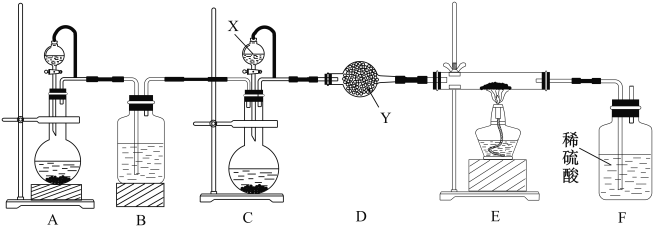
设计实验步骤如下:
①滴加几滴NiCl2 溶液润湿金属镓粉末,置于反应器内。
②先通入一段时间后的H2,再加热。
③停止通氢气,改通入氨气,继续加热一段时间。
④停止加热,继续通入氨气,直至冷却。
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应过滤、洗涤、干燥。
(1)仪器X中的试剂是___________,仪器Y的名称是__________________。
(2)指出该套装置中存在一处明显的错误是________________________。
(3)步骤①中选择NiCl2 溶液,不选择氧化镍的原因是____________________。
a.增大接触面积,加快化学反应速率
b使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,则判断该反应接近完成时观察到的现象是____________________。
(5)请写出步骤⑤中检验产品氮化镓固体洗涤干净的操作________________________。
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热NaOH溶液的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性强弱:I- >Fe2+。往100 mL碘化亚铁溶液中缓慢通入3.36 L(标准状况)氯气,反应完成后溶液中有1/2的Fe2+被氧化成Fe3+。则原碘化亚铁溶液的物质的量浓度为
A. 1.1mol·L-1 B. 1.5mol·L-1 C. 1.2mol·L-1 D. 1.0mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com