
【题目】在反应中乙醇分子会断裂C—O键的是( )
A. 乙醇与丁酸的取代反应 B. 乙醇与金属钠反应
C. 乙醇在浓硫酸存在下发生消去反应 D. 乙醇在铜丝存在条件下发生催化氧化
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】偏二甲肼(C2H8N2)是一种高能液态燃料,其燃烧产生的巨大能量可作为航天运载火箭的推动力。下列叙述正确的是
A. NA个偏二甲肼分子的质量为60g
B. 标准状况下,1mol偏二甲肼的体积约为22.4L
C. 偏二甲肼的摩尔质量为60g
D. 6g偏二甲肼分子中含有0.1NA个N2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲配制80mL2.0mol/LNaOH溶液,其转移溶液的操作如图所示。
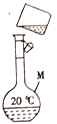
(1)图中操作上的错误是________。
(2)图中用到的仪器M是_______(填仪器名称和规格),下列关于仪器M的使用方法中,正确的是_______ (填字母)。
a.使用前应检查是否漏液 b.使用前必须烘干
c.不能用作物质反应或溶解的容器 d.可直接将热溶液转移到其中
(3)该同学称取NaOH固体的质量为________。
(4)下列操作会使配制的溶液浓度偏高的是______(填字母)。
a.所用过的烧杯未洗涤
b.转移过程中有少量溶液溅出
c.摇匀后,液面下降,再加入水至刻度线
d.定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乌洛托品在合成、医药、染料等工业中有广泛用途,其结构式如图所示。将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比为( )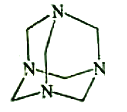
A. 1:1 B. 2:3 C. 3:2 D. 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017北京]某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到Fe3+,发现和探究过程如下。
向硝酸酸化的0.05 mol·L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物
①取出少量黑色固体,洗涤后,_______(填操作和现象),证明黑色固体中含有Ag。
②取上层清液,滴加K3[Fe(CN)6]溶液,产生蓝色沉淀,说明溶液中含有_______________。
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是___________________(用离子方程式表示)。针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
序号 | 取样时间/min | 现象 |
ⅰ | 3 | 产生大量白色沉淀;溶液呈红色 |
ⅱ | 30 | 产生白色沉淀;较3 min时量少;溶液红色较3 min时加深 |
ⅲ | 120 | 产生白色沉淀;较30 min时量少;溶液红色较30 min时变浅 |
(资料:Ag+与SCN-生成白色沉淀AgSCN)
② 对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于________(用离子方程式表示),可产生Fe3+;
假设c:酸性溶液中![]() 具有氧化性,可产生Fe3+;
具有氧化性,可产生Fe3+;
假设d:根据_______现象,判断溶液中存在Ag+,可产生Fe3+。
③ 下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因。实验Ⅱ可证实假设d成立。
实验Ⅰ:向硝酸酸化的________溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液,3 min时溶液呈浅红色,30 min后溶液几乎无色。
实验Ⅱ:装置如图。其中甲溶液是________,操作及现象是________________。

(3)根据实验现象,结合方程式推测实验ⅰ~ⅲ中Fe3+浓度变化的原因:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【天津市和平区2017届第三次质量调查(三模)】A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一。请化学用语回答下列问题:
(1)F在元素周期表中的位置为_______________。
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为_______________。
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。H的电子式为_______,写出在空气中长期放置生成H的化学反应方程式为:_________。H的溶液与稀硫酸反应产生的现象为_____________。
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol A4B4熔融电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________。
(5)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。
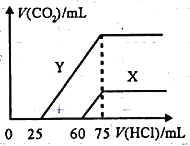
则曲线Y表明M中的溶质为________;原NaOH溶液的物质的量浓度为_______;由曲线X、Y可知,两次实验通入的CO2的体积比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是( )
A. 1mol NH4+含有的电子数目为11NA
B. 常温常压下,1.38g K2CO3含有的K+离子数为0.02NA
C. 标准状况下,11.2L CCl4含有的分子数为0.5NA
D. 100 mL 0.1 mol/LCH3COOH溶液中含有的H+离子数为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能与溴水发生反应的是①苯 ②苯酚③亚硫酸④NaOH溶液⑤AgNO3溶液⑥裂化汽油⑦己烷⑧镁粉( )
A. ①③⑦ B. ①④⑧ C. ①⑦ D. ②⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在苯的同系物中加入少量KMnO4酸性溶液,振荡后褪色,正确的解释为( )
A.苯的同系物分子中的碳原子数比苯分子中的碳原子数多
B.苯环受侧链影响易被氧化
C.侧链受苯环影响易被氧化
D.由于苯环和侧链的相互影响均易被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com