
【题目】A、B的混合气体在密闭容器中发生如下反应:xA(g)+yB(g) ![]() zC(g) △H<0。
zC(g) △H<0。
达到化学平衡后测得A的浓度为0.5 mol·L-1;在恒温下,将密闭容器的容积压缩至
原来的二分之一,再次达到平衡时,测得A的浓度为0.9 mol·L-1。则下列叙述中
正确的是( )
A. 平衡向正反应方向移动了 B. x+y<z
C. B的转化率下降 D. C的体积分数减小
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A. AgCl>AgI>Ag2CrO4 B. AgCl>Ag2CrO4>AgI
C. Ag2CrO4>AgCl>AgI D. Ag2CrO4>AgI>AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.加入苯酚显紫色的溶液:K+、NH4+、Cl﹣、I﹣;加入酚酞呈红色的溶液:SO42﹣、K+、Cl﹣、HSO3﹣分别都不能大量共存(常温下)
B.![]() =1×10﹣12的溶液:K+、AlO2﹣、CO32﹣、Na+; pH=2的溶液:NO3﹣、Fe2+、Na+、Al3+分别都可以大量共存(常温下)
=1×10﹣12的溶液:K+、AlO2﹣、CO32﹣、Na+; pH=2的溶液:NO3﹣、Fe2+、Na+、Al3+分别都可以大量共存(常温下)
C.已知:25℃时,Mg(OH)2的Ksp=5.61×10﹣12 , MgF2的KSP=7.42×10﹣11 , 25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2 可以转化为MgF2
D.表示H2燃烧热的化学方程式为:H2(g)+ ![]() O2(g)═H2O(1);△H=﹣285.8kJ/mol
O2(g)═H2O(1);△H=﹣285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产生活中应用广泛,请解决下列问题.
(1)硫酸铜溶液时白磷引起中毒的一种解毒剂:
P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4 , 若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为 .
(2)氮的化合物合成、应用及氮的固定一直是科学研究的热点.以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=﹣159.47kJmol﹣1
②NH2CO2NH4(s)=CO (NH2)2(s)+H2O(g);△H=a kJmol﹣1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);△H=﹣86.98kJmol﹣1
则a为 .
(3)如图表示使用新型电极材料,以N2、H2为电极反应物,以HCl﹣NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池.请写出该电池的正极反应式 . 生产中可分离出的物质A的化学式为 . 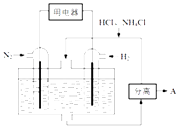
(4)常温下,向0.1mol/L氨水中加入少许N2O5 , 使溶液中c(NH3H2O):c(NH4+)=5:9,此时溶液的pH= . (25℃时,NH3H2O的电离常数Kb=1.8×10﹣5)
(5)SiO2溶于氢氟酸后生成一种极强的二元酸和水,经分析该酸由3种元素组成,其中氟严肃的质量分数为79.17%.请写出SiO2溶于氢氟酸的离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图,下列说法不正确的是( )
A.拆开2molH2(g)和1molO2(g)中的化学键成为H、O原子,共吸收1368kJ能量
B.由H、O原子形成2molH2O(g),共放出1852kJ能量
C.2molH2(g)和1molO2(g)反应生成2molH2O(g),共吸收484kJ能量
D.2molH2(g)和1molO2(g)反应生成2molH2O(g),共放出484kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2 mol SO2和2 mol SO3气体混合于某固定体积的密闭容器中,在一定条件下反应:2SO2(g)+O2(g)![]() 2SO3(g),平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3的物质的量大于W mol的是( )
2SO3(g),平衡时SO3为W mol。相同温度下,分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3的物质的量大于W mol的是( )
A.2 mol SO2+1 mol O2B.4 mol SO2+1 mol O2
C.2 mol SO2+1 mol O2+2 mol SO3D.3 mol SO2+1 mol SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数,下列叙述正确的是( )
A.24g镁的原子最外层电子数为NA
B.1L 0.1molL﹣1乙酸溶液中H+数为0.1NA
C.1mol甲烷分子所含质子数为10NA
D.标准状况下,22.4L乙醇的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
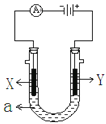
(1)若X、Y都是石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:①电解池中X极上的电极反应式为_______________________,在X极附近观察到的现象是___________________。
②Y电极上的电极反应式为__________________________,一段时间后电解质溶液中看到的实验现象是_________________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是_______________,电极反应式是______________________。
②Y电极的材料是______________,电极反应式是__________________。(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com