
【题目】设NA为阿伏伽德罗常数,下列叙述正确的是( )
A.24g镁的原子最外层电子数为NA
B.1L 0.1molL﹣1乙酸溶液中H+数为0.1NA
C.1mol甲烷分子所含质子数为10NA
D.标准状况下,22.4L乙醇的分子数为NA
科目:高中化学 来源: 题型:
【题目】某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式: .
(2)实验结果表明,催化剂的催化效果与有关.
(3)某同学在10mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A,B,C三点所表示的反应速率最慢的是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝碱式酸盐[MgaAlb(OH)c(CO3)dxH2O]阻燃剂具有阻燃、消烟、填充等功能,是一种不溶于水的新型无机阻燃剂.
(1)将[MgaAlb(OH)c(CO3)dxH2O]表示成氧化物形式.
(2)为确定镁铝碱式碳酸盐的组成,进行如下实验:
准确称取15.050g样品进行灼烧至恒重,生成CO20.560L(已换算成标准状况下).分析测得残留物中MgO为6.000g,Al2O3为2.550g,通过计算确定该镁铝碱式碳酸盐的化学式 . (写出计算过程)
(3)该镁铝碱式碳酸盐可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,制备的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B的混合气体在密闭容器中发生如下反应:xA(g)+yB(g) ![]() zC(g) △H<0。
zC(g) △H<0。
达到化学平衡后测得A的浓度为0.5 mol·L-1;在恒温下,将密闭容器的容积压缩至
原来的二分之一,再次达到平衡时,测得A的浓度为0.9 mol·L-1。则下列叙述中
正确的是( )
A. 平衡向正反应方向移动了 B. x+y<z
C. B的转化率下降 D. C的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①试管 ②坩埚 ③量筒 ④蒸发皿 ⑤烧瓶 ⑥集气瓶 ⑦烧杯 ⑧漏斗,可以用酒精灯直接加热的是
A. ①②③④⑤⑧ B. ①②④
C. ①③⑥⑦⑧ D. 都能直接加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Cl﹣、SO42﹣、CO32﹣、NH4+、Fe3+、Al3+和K+ . 取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
A.至少存在5种离子
B.Cl﹣一定存在,且c(Cl)≥0.4mol/L
C.SO42﹣、NH4+、一定存在,Cl﹣可能不存在
D.CO32﹣、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题: 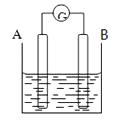
(1)若电流表的指针偏向B,则A为极,B为极
(2)若电流表G发生偏转,同时A极质量增加,B极质量减少,C为电解质溶液.则A、B、C分别为
A.A是Zn,B是Cu,C是稀硫酸
B.A是Cu,B是Zn,C是稀硫酸
C.A是Fe,B是Ag,C是稀AgNO3溶液
D.A是Ag,B是Fe,C是稀AgNO3溶液
(3)若电解质溶液是稀硫酸,按此图组装后,观察到A极不断的溶解,B极有气泡冒出,则A,B的金属性强弱为
(4)任何一个自发的氧化还原反应都可以设计为原电池,若该电池中发生的反应为:Fe+2FeCl3═3FeCl2 , A电极为铁,则B电极为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于过滤和蒸发的说法错误的是
A.过滤时漏斗下端须紧靠烧杯内壁
B.过滤时滤纸边缘要低于漏斗边缘
C.蒸发时要用玻璃棒不断搅拌液体
D.蒸发时将液体全部蒸干后停止加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图,回答下列问题: 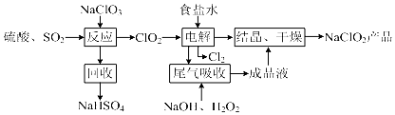
(1)ClO2的沸点为283K,纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下更安全.写出“反应”步骤中生成ClO2的化学方程式 .
(2)“尾气吸收”是吸收“电解”过程排出的少量ClO2 .
①在尾气吸收过程中,可代替H2O2的试剂是(填序号).
A.Na2O2B.Na2S C.FeCl2D.KMnO4
②提高尾气的吸收效率的可行措施有(填序号).
A.尾气吸收时充分搅拌吸收液B.适当加快尾气的通入速率C.将温度控制在20℃以下D.加水稀释尾气吸收液
③此吸收反应中,氧化剂与还原剂的物质的量之比为 .
(3)在碱性溶液中NaClO2比较稳定,在酸性溶液中,ClO2﹣和H+合为HClO2 , HClO2
是唯一的亚卤酸,不稳定,易分解产生Cl2、ClO2和H2O,写出HClO2分解的化学方程式: .
(4)已知NaClO2的溶解度随温度升高而增大,NaClO2饱和溶液在38℃以上60℃以下会析出NaClO2 , 在NaClO2析出过程中可能混有的杂质是(填化学式).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com