
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
分析 探究温度对化学反应速率的影响,应选择浓度相同条件下的实验;要探究浓度对化学反应速率的影响,应选择温度相同条件下的实验;
实验①、实验②和实验③的温度相同,浓度不同,反应物的浓度为变量,据此解答.
解答 解:探究温度对化学反应速率的影响,应选择浓度相同条件下的实验,所以应选择①⑤或②④;要探究浓度对化学反应速率的影响,应选择温度相同条件下的实验,所以应选择①②或①③或④⑤;实验①、实验②和实验③的温度相同,浓度不同,因此探究的是浓度对化学反应速率的影响,
故答案为:①⑤或②④;①②或①③或④⑤;比较改变不同反应物的浓度对反应速率的影响.
点评 本题考查外界条件对化学反应速率的影响,探究单一条件对速率的影响时,要让此条件成为唯一变量,整体难度适中.


科目:高中化学 来源: 题型:解答题
| 化学键 | H-Cl | Cl-Cl | H-H | C-H | C-Cl |
| 键能/(kJ•mol-1) | 431.4 | 242.1 | 435.9 | 413.0 | 338.9 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:选择题
下列有关气体体积的叙述中,正确的是
A.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定
B.不同的气体,若体积不同,则它们所含的分子数也不同
C.一定温度和压强下,各种气体体积大小,由构成气体分子的大小决定
D.气体摩尔体积就是1mol任何气体所占体积都约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 待测NaOH溶液的体积/mL | 滴定完成时,消耗盐酸的体积/mL |
| 1 | 20.00 | 22.40 |
| 2 | 20.00 | 22.42 |
| 3 | 20.00 | 22.38 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
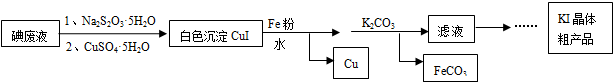
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
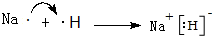 .
.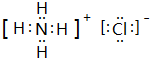 ,A2C2的电子式为
,A2C2的电子式为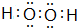 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
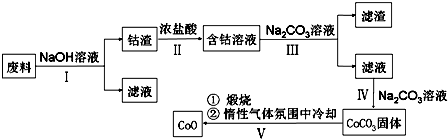
| A. | 第Ⅰ步反应后得到的滤液主要是含铝溶液 | |
| B. | 第Ⅱ步中盐酸表现出酸性、还原性,且必须过量 | |
| C. | 第Ⅲ步中Na2CO3主要作用是使Fe3+沉淀,滤渣主要为Fe(OH)3 | |
| D. | 第Ⅳ步操作为过滤,第Ⅴ步煅烧后,也可以在一氧化碳气体氛围中冷却 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入Al能放出H2的溶液中:NH4+,SO42-,Br-,NO3- | |
| B. | 通入过量SO2气体的溶液中:Fe3+、NO3-、Ba2+、H+ | |
| C. | 无色强酸性溶液中:Na+、Cl-、SO42-、Cu2+ | |
| D. | c(I-)=0.1 mol•L-1的溶液中:Na+、Fe2+、Cl-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com