
| A. | HClO的结构式:H-O-Cl | |
| B. | 比例模型: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 | |
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| D. | NH4Cl的电子式: |
分析 A、次氯酸的中心原子是氧原子,根据成键情况来书写结构式;
B、比例模型既能表示分子的空间结构,又能表示出分子中各原子的相对大小,与分子的真实结构最接近;
C、质量数=质子数+中子数;
D、阴离子的电子式应表示出最外层电子.
解答 解:A、次氯酸的中心原子是氧原子,结构式为H-O-Cl,故A正确;
B、甲烷结构和四氯化碳结构不同类似,但由于氯原子比碳原子大,但H原子比碳原子小,故两者的比例模型不同,故B错误;
C、质量数=质子数+中子数,故中子数为20的氯原子为3717Cl,故C错误;
D、阴离子的电子式应表示出最外层电子,故氯化铵的电子式为: ,故D错误.
,故D错误.
故选A.
点评 本题考查了常见的化学用语的书写,难度不大,应注意的是HClO中H、Cl、O原子间的成键情况.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:推断题
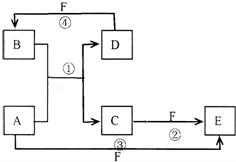 已知A、B、C、D、E、F六种物质的转化关系如图所示 (反应条件和部分产物未标出)
已知A、B、C、D、E、F六种物质的转化关系如图所示 (反应条件和部分产物未标出) ,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2+2H2O═CH4+2O2 | B. | NaOH+HCl═NaCl+H2O | ||
| C. | 4Al+3O2+6H2O═4Al(OH)3 | D. | Cu+2HCl═CuCl2+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型: | |
| B. | 羟基的电子式: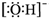 | |
| C. | 乙烯的结构简式:CH2CH2 | |
| D. | 中子数为54、质子数为92的铀原子14692U |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4和C3H6一定属于同系物 | |
| B. | 淀粉[(C6H10O5)n]与纤维素[(C6H10O5)n]互为同分异构体 | |
| C. | 同系物之间化学性质相似,物理性质递变 | |
| D. | 同分异构体之间化学性质相似,物理性质递变 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 已知碳碳单键可以绕键轴自由旋转,分子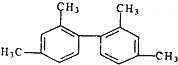 中至少有9个碳原子处于同一平面上 中至少有9个碳原子处于同一平面上 | |
| B. | 取W克乙烯和丙烯的混合气体,使之充分燃烧时,耗氧量跟混合物中各组分的质量比无关 | |
| C. | 在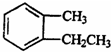 的同分异构体中,苯环上的一氯代物有两种结构的只有1种 的同分异构体中,苯环上的一氯代物有两种结构的只有1种 | |
| D. | 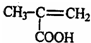 的核磁共振氢谱有3种峰,其峰面积之比为3:2:1 的核磁共振氢谱有3种峰,其峰面积之比为3:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 向NaOH溶液中滴加少量AlCl3溶液:Al3++3OH-=Al(OH)3↓ | |
| C. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O=H2SiO3↓+CO32- | |
| D. | 将NaHSO4与Ba(OH)2溶液混合至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com