
����Ŀ�����������Ȼ��������Ҫ�Ļ����Լ������ǵ�һЩ���ʼ��Ʊ�����������ʾ��
�����Ȼ������۵�Ϊ306�����е�Ϊ315���������տ����е�ˮ�ֶ����⡣��ҵ�ϲ�����500��600 ����������ͨ��������������ˮ�Ȼ�����
�����Ȼ��������۵�Ϊ670 ��������������ҵ�ϲ��������������ͨ���Ȼ�����������ˮ�Ȼ�������
ʵ���ҿ�����ͼ��ʾ��װ��ģ�ҵ������ˮ�Ȼ�������ش�������⣺
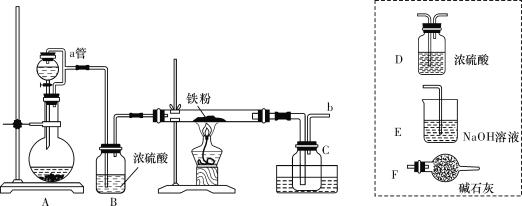
(1)װ��A����KMnO4������Ũ���ᷴӦ����������Ӧ�����ӷ���ʽΪ_______��
(2)����b��Ӧ��_______(�����߿���װ����ѡ��װ�ú�����ĸ�������)���ӣ������ɱ��ⷴӦϵͳ�뻷������Ӱ�졣
(3)ʵ����ɺ�ȡ���ƿC���ռ����IJ���������²ⶨ�ٳ�ȡ4.52 g��Ʒ���ڹ�����ϡ�����У��ڼ�������H2O2�����ټ�������NaOH��Һ���ܹ��ˡ�ϴ�Ӻ����ճ������ݳ������ú���ɫ����Ϊ2.40 g�������Ʒ����Ԫ�ص���������Ϊ___________%(�����ȷ��С�������λ)��
(4)���������ݷ����ͼ���ó����ۣ�
���ô�װ���Ƶõ���ˮ�Ȼ���������______(����ƫ��������ƫ����)����Ȼ���к��н϶��__________(�ѧʽ)���ʡ�
����Ҫ�õ��ϴ�������ˮ�Ȼ������ɲ�ȡ��װ�øĽ���ʩ��_________________��
���𰸡�2MnO4-��10Cl����16H��=2Mn2����5Cl2����8H2O F 37.17 ƫ�� FeCl2 ��װ��A��B���װһ��ʢ�б���ʳ��ˮ��ϴ��ƿ
��������
ʵ�����ͼ������Fe��Cl2��Ӧ��ȡFeCl3��Cl2��KMnO4��Ũ���ᷴӦ�Ƶã�����Ũ�����ӷ����Ȼ��⣬����Cl2�л���HCl��ˮ�������ñ���ʳ��ˮ��ȥ�Ȼ��⣬��Ũ����ȥ��ˮ����������ȥ��HCl����Fe��HCl��Ӧ����FeCl2����FeCl3�У�Cl2�ж�������Ⱦ������Ӧ�ü�Һ���գ����⣬FeCl3������ˮ�⣬�����ռ�װ����Ӧ��ֹˮ�����Ľ��롣
(1)װ��A����KMnO4������Ũ���ᷴӦ��������������Ӧ�Ļ�ѧ����ʽΪ2KMnO4+16HCl(Ũ)=2KCl+2MnCl2+5Cl2��+8H2O�����ӷ���ʽΪ2MnO4-��10Cl����16H��=2Mn2����5Cl2����8H2O��
����2MnO4-��10Cl����16H��=2Mn2����5Cl2����8H2O��
(2)��ʯ��Ϊ������������ʯ�ҵĻ����ܹ���������Ӧ��Ҳ�ܹ�����ˮ�������������壻β������ʱ����Ҫ����Cl2�ij�����գ���Ҫ���Ƿ�ֹˮ��������װ���ڣ�ʹ�Ȼ�������ˮ�⣬����Ӧѡ��Fװ�ã��Ӷ�ȷ������b��Ӧ��F���ӣ�
����F��
(3)m(Fe2O3)=2.40g��n(Fe)=![]() =0.03mol������Ʒ����Ԫ�ص���������Ϊ
=0.03mol������Ʒ����Ԫ�ص���������Ϊ![]() =37.17%��
=37.17%��
����37.17��
(4)����ΪCl2�е�HCl��Fe��Ӧ����FeCl2������FeCl3�У������ô�װ���Ƶõ���ˮ�Ȼ���������ƫ�ߣ���Ȼ���к��н϶��FeCl2��
��Ϊ��ƫ�ߣ�FeCl2��
����Ҫ�õ��ϴ�������ˮ�Ȼ�����Ӧ��Cl2����ǰ����ȥCl2���е�HCl���ɲ�ȡ��װ�øĽ���ʩ����װ��A��B���װһ��ʢ�б���ʳ��ˮ��ϴ��ƿ��
��Ϊ����װ��A��B���װһ��ʢ�б���ʳ��ˮ��ϴ��ƿ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС������֤��Ӧ��Fe+2Ag+=Fe2++2Ag����ʵ���м�Fe3+�����ֺ�̽���������¡�
�������ữ��0.05mol��L-1��������Һ��pH��2���м���������ۣ�������ã��ձ��ײ��к�ɫ���壬��Һ�ʻ�ɫ��
��1���������
��ȡ��������ɫ���壬ϴ�Ӻ�__�������������֤����ɫ�����к���Ag��
��ȡ�ϲ���Һ���μ�K3Fe(CN)6��Һ��������ɫ������˵����Һ�к���__��
��2���������Һ�ʻ�ɫ��������Ϊ��Һ����Fe3+������Ϊ���۹���ʱ��������Fe3+�������ݵ�ԭ����__�������ӷ���ʽ��ʾ����������ֹ۵����ʵ�飺
��ȡ�ϲ���Һ���μ�KSCN��Һ����Һ��죬֤ʵ�˼IJ²⡣ͬʱ�����а�ɫ��������������Һ��ɫ��dz��������������ȡ��ʱ���йأ��Ա�ʵ���¼���£�
��� | ȡ��ʱ��/min | ���� |
�� | 3 | ����������ɫ��������Һ�ʺ�ɫ |
�� | 30 | ������ɫ��������3minʱ���٣���Һ��ɫ��3minʱ���� |
�� | 120 | ������ɫ��������30minʱ���٣���Һ��ɫ��30minʱ��dz |
�����ϣ�Ag+��SCN-���ɰ�ɫ����AgSCN��
�ڶ�Fe3+������ԭ���������¼��裺
����a�����������۱����������㣬�ܲ���Fe3+��
����b�������д���O2������__�������ӷ���ʽ��ʾ�����ɲ���Fe3+��
����c��������Һ��NO3-���������ԣ��ɲ���Fe3+��
����d������__�����ж���Һ�д���Ag+���ɲ���Fe3+��
������ʵ����֤ʵ����a��b��c���Dz���Fe3+����Ҫԭ��ʵ����֤ʵ����d������
ʵ����������ữ��__��Һ��pH��2���м���������ۣ�������ã���ͬʱ��ȡ�ϲ���Һ�μ�KSCN��Һ��3minʱ��Һ��dz��ɫ��30min����Һ������ɫ��
ʵ���װ����ͼ�����м���Һ��__��������������__��
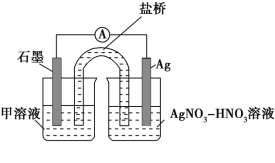
��3������ʵ������Ϸ���ʽ�Ʋ�ʵ�颡~����Fe3+Ũ�ȱ仯��ԭ��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ʽ��д�������
A.�Ҵ���������ȡ��ȩ��2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
B.��ϩʹ������Ȼ�̼��Һ��ɫ��CH2=CH2+Br2��CH2Br��CH2Br
C.CH4��Cl2��Ϻ���գ�CH4��Cl2![]() CH2Cl2��H2
CH2Cl2��H2
D.������Ҵ�������Ӧ��������������CH3CH2OH+CH3COOH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����K2Cr2O7��Һ����FeSO4��Һ��Ӧ����Fe3����Cr3�����ֽ������ữ��K2Cr2O7��Һ��FeSO4��Һ��ϣ���ַ�Ӧ������������Һ�м���KI��Һ�������Һ��Fe3�������ʵ���������KI�����ʵ����ı仯��ϵ��ͼ��ʾ������˵���в���ȷ����
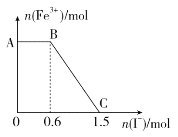
A. ͼ��AB�ε�������ΪK2Cr2O7
B. ��ʼ�����K2Cr2O7Ϊ0.25 mol
C. K2Cr2O7��FeSO4��Ӧ�����ʵ���֮��Ϊ1��3
D. ͼ��BC�η����ķ�ӦΪ2Fe3����2I��===2Fe2����I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijЩ������ΪNO������Na2O2��Ӧ����ͬѧ������ɣ�����ΪNO����O2������Ӧ��Ӧ�ø����ױ�Na2O2������
�������ϣ�a.2NO��Na2O2=2NaNO2
b��6NaNO2��3H2SO4(ϡ)=3Na2SO4��2HNO3��4NO����2H2O
c�����������£�NO�ܱ�MnO4��������NO3��
��ͬѧ������ͼ��װ����̽��NO��Na2O2�ķ�Ӧ(װ�ÿ��ظ�ʹ��)��
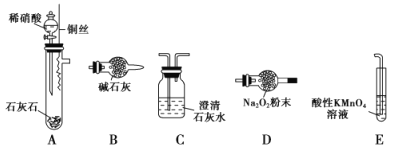
(1)װ�����ӵ�˳��ΪA��_______________��A������NO�Ļ�ѧ����ʽ____________��
(2)װ��C��������_________________��
(3)װ��E��������_________________��������Ӧ�����ӷ���ʽΪ______________��
(4)��ַ�Ӧ����Dװ�����Ƿ�������NaNO2��ʵ�������______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵���������
A.3.6 g C60��C50��ɵĻ�����С����еĵ�����ĿΪ1.8NA
B.6.72 L(��״��)Cl2���������鷴Ӧʱ�����ѵ�C-H����ĿΪ0.3NA
C.0.1 LŨ�Ⱦ�Ϊ2 mol/L��(NH4)2SO4��NH4Cl��Һ�У�NH4+��Ŀǰ�߱Ⱥ��߶�0.2 NA
D.0.1 mol H3BO3[���뷽��ʽ��H3BO3+H2O![]() H++B(OH)4-]����OH-��Ŀ���Ϊ0.1 NA
H++B(OH)4-]����OH-��Ŀ���Ϊ0.1 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����������ڷǻ�ԭ���ǣ�����ˮ�������л�ԭ�Ե�ʵ�鷽����˵���У���ȷ����
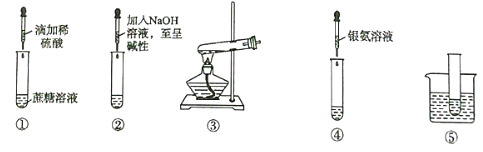
A. ��֤�������ڷǻ�ԭ���ǵIJ���˳�ܢ�
B. ��֤�������ڷǻ�ԭ���ǵIJ���˳�ۢ�
C. ��֤����ˮ�������л�ԭ�ԵIJ���˳�٢ܢ�
D. ��֤����ˮ�������л�ԭ�ԵIJ���˳�٢ݢڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ�Ϊ2 L���ܱ�������, ijһ��Ӧ������M������N�����ʵ����淴Ӧʱ��仯��������ͼ��ʾ, �����ͼʾ�ش��������⡣
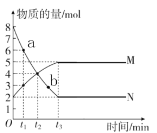
(1)д���÷�Ӧ�Ļ�ѧ����ʽ��____________��
(2)t1��t3ʱ��Σ���M��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ________(�ú�t1��t3��ʽ�ӱ�ʾ)��
(3)�Ƚ�a����b�㷴Ӧ���ʴ�С��Va___Vb(����>����=�� �� ��< ��)��
(4)��ͼ��ʾ������ʱ���У�___________(��t1��t2��t3)ʱ�̴���ƽ��״̬��
(5)���������У���˵���÷�Ӧ�ﵽƽ��״̬����________��
A��������M��N�����ʵ������
B��������M��N��Ũ�Ȳ���ʱ��仯
C����λʱ����ÿ����1 mol N��ͬʱ����0.5 mol M
D��������ѹǿ����ʱ��仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ҫ�Ļ���ԭ�ϣ�����ú������������CO��CO2��H2����ȡ�״����л�������ķ�Ӧ�У�
��CO(g)+2H2(g)![]() CH3OH(g) ��H1=��99kJmol-1
CH3OH(g) ��H1=��99kJmol-1
��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H2
CH3OH(g)+H2O(g) ��H2
������ʵĻ�ѧ�������������£�CH3OH�ṹʽ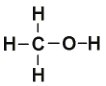
��ѧ�� | C=O(CO2) | H��H | C��O | H��O | C��H |
E/(kJ��mol-1) | 803 | 436 | 343 | 465 | 413 |
(1)�÷�Ӧ��H2=____________��
(2)���ڷ�Ӧ������˵������ȷ����____________��
A.�÷�Ӧ���κ��¶��¶����Է�����
B.�����¶ȣ�����Ӧ���������淴Ӧ���ʼ�С
C.ʹ�ô������������CO��ת����
D.����ѹǿ���÷�Ӧ�Ļ�ѧƽ�ⳣ������
(3)��ij�¶��£���1.0moCO��2.0molH2����2L�Ŀո�ƿ�У�������Ӧ�٣��ڵ�5minʱ�ﵽ��ѧƽ��״̬����ʱ�״������ʵ�������Ϊ0.1���ڵ�10min��20minʱ�ֱ�ı䷴Ӧ�������״���Ũ���ڲ�ͬ�����µı仯״����ͼ��ʾ��

�ٴӷ�Ӧ��ʼ��5minʱ�����ɼ״���ƽ������Ϊ____________��
��H2��ƽ��ת������=____________%����ѧƽ�ⳣ��K=____________��
��1minʱ������____________����(����ڡ���С�ڡ����ڡ�)
��1mimʱ����____________4minʱ����(����ڡ���С�ڡ����ڡ�)
�ݱȽϼ״���7��8min��12��13min��25��27minʱƽ����Ӧ����[ƽ����Ӧ���ʷֱ�����(7��8)����(12��13)����(25��27)��ʾ�Ĵ�С____________��
��������ƿ����ͬ�ݻ��ľ����������ظ��������飬ƽ��ʱ�״������ʵ�������____________0.1(�>������<����=��)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com