
【题目】Ⅰ.某化学兴趣小组用FeCl2(用铁粉与盐酸反应制得)和NH4HCO3制备FeCO3的装置示意图如图所示。回答下列问题:

(1)A装置的名称是____________;FeCO3在________中生成(填字母),该装置中发生的主要反应的离子方程式为____________________。
(2)实验时首先打开活塞3,关闭活塞2,其目的是___________________;然后再关闭活塞3,打开活塞2,其目的是_____________________。
Ⅱ.乳酸亚铁晶体([CH3CH(OH)COO]2Fe·3H2O,Mr=288)是常用的补铁剂。乳酸亚铁可由乳酸与碳酸亚铁反应制得。
(3)将制得的FeCO3加入乳酸溶液中,再加入过量铁粉,75℃下搅拌使之充分反应。结束后,无需过滤,除去过量铁粉的反应方程式为_____________。
(4)从上述(3)所得溶液中获得乳酸亚铁晶体的方法是___________________、___________________、洗涤、干燥。
(5)该兴趣小组用KMnO4测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是_______________。经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880 g产品配成100 mL溶液,每次取20.00 mL,进行必要处理,用0.100 0 mol·L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)219.7 mL。滴定反应为Ce4++Fe2+====Ce3++Fe3+,则产品中乳酸亚铁晶体的质量分数为____________。
【答案】(1)长颈漏斗,C;Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;
(2)排出装置中的空气,防止+2价铁被氧化; 使B装置中气压增大,将B装置中的氯化亚铁溶液压入C中;
(3)2CH3CH(OH)COOH+Fe![]() [CH3CH(OH)COO]2Fe+H2↑;
[CH3CH(OH)COO]2Fe+H2↑;
(4)冷却结晶 过滤;(5)乳酸根离子中含有羟基,能被酸性高锰酸钾溶液氧化,98.5%。
【解析】
试题分析:(1)A装置是分液漏斗,装置B的是制取FeCl2,然后关闭止水夹3,利用气体压强把FeCl2压入到装置C中,因此FeCO3在装置C中生成,发生反应是Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;(2)Fe2+容易被氧气氧化,因此操作的目的是排除装置中空气,防止Fe2+被氧化;此操作的目的使B装置中气压增大,将B装置中的氯化亚铁溶液压入C中;(3)加入过量的乳酸,让过量铁和乳酸继续反应,其反应方程式为2CH3CH(OH)COOH+Fe[CH3CH(OH)COO]2Fe+H2↑;(4)乳酸亚铁晶体中含有结晶水,因此采用蒸发浓缩,冷却结晶、过滤的方法;(5)乳酸根离子中含有羟基,能被酸性高锰酸钾溶液氧化,根据得失电子守恒,19.7×10-3×0.1××100×1/20=n(Fe2+)×1,解得n(Fe2+)=9.85×10-3mol,乳酸亚铁的质量分数为9.85×10-3×288/2.88×100%=98.5% 。


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:
【题目】微量元素是指每种质量不到体重的万分之一,质量总和不到人体质量的千分之一的近二十种元素,这些元素对人体正常代谢和健康起着重要作用。下列元素不是微量元素的是( )
A.I B.H C.Zn D.Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,既属于氧化还原反应同时又是吸热反应的是( )
A. Ba(OH)28H2O与NH4Cl反应 B. 灼热的碳与高温水蒸气的反应
C. 铝与稀盐酸 D. H2与O2的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子或分子组中能大量共存,且满足相应要求的是
选项 | 离子或分子 | 要求 |
A | K+、NO | c(K+)<c(Cl-) |
B | Fe3+、NO | 滴加盐酸立即有气体产生 |
C | NH | 滴加NaOH溶液立即有气体产生 |
D | Na+、HCO | 滴加氨水立即有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(图中夹持装置均已略去)。
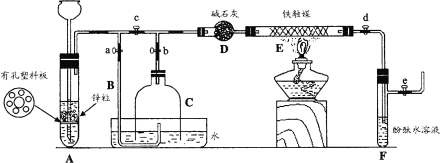
[实验操作]
① 检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气发生。在F出口处收集氢气并检验其纯度。
② 关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③ 用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是 。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是 ,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是 ,C瓶内气体的成份是 。
(3)在步骤③中,先加热铁触媒的原因是 。反应管E中发生反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的气化可以减少环境污染,而且生成的CO和H2被称作合成气,能合成很多基础有机化工原料。
(1)工业上可利用CO生产乙醇:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) ΔH1
CH3CH2OH(g)+H2O(g) ΔH1
又知:H2O(l)=H2O(g) ΔH2
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
工业上也可利用CO2(g)与H2(g)为原料合成乙醇:
2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(l) ΔH
CH3CH2OH(g)+3H2O(l) ΔH
则ΔH与ΔH1、ΔH2、ΔH3之间的关系是ΔH=____________。
(2)一定条件下,H2、CO在体积固定的绝热密闭容器中发生如下反应:4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g),下列选项不能判断该反应达到平衡状态的是__________。
CH3OCH3(g)+H2O(g),下列选项不能判断该反应达到平衡状态的是__________。
A.v(H2)正=2v(CO)逆 B.平衡常数K不再随时间而变化
C.混合气体的密度保持不变 D.CH3OCH3和H2O的体积之比不随时间而变化
(3)工业可采用CO与H2反应合成再生能源甲醇,反应:CO(g)+2H2(g)![]() CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图1所示。
CH3OH(g),在一容积可变的密闭容器中充有10 mol CO和20 mol H2,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图1所示。
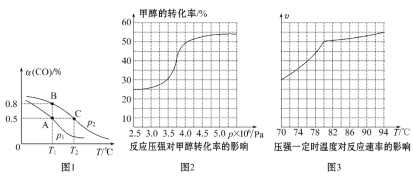
①合成甲醇的反应为______________(填“放热”或“吸热”)反应。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为____________________。p1和p2的大小关系为___________。
③若达到平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积为________L。
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为CH3OH(g)+CO(g)![]() HCOOCH3(g) ΔH2=-29.1 kJ·mol-1。科研人员对该反应进行了研究,部分研究结果如图2、3:
HCOOCH3(g) ΔH2=-29.1 kJ·mol-1。科研人员对该反应进行了研究,部分研究结果如图2、3:
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是________(填“3.5×106Pa”“4.0×106Pa”或“5.0×106Pa”)。
②实际工业生产中采用的温度是80℃,其理由是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对二氧化硫气体的物理性质或化学性质描述正确的有
A.无色、无味 B.容易液化、难溶于水
C.有漂白性,能使品红溶液褪色 D.和水反应生成硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关二氧化碳的说法错误的是( )
A. 在空气中二氧化碳的体积分数约为0.03%
B. 二氧化碳有毒,不能供人呼吸
C. 过多的二氧化碳排放会导致温室效应
D. 干冰可用于人工降雨
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com