
科目:高中化学 来源:必修一导学指导化学鲁科版 鲁科版 题型:022
| |||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)氯气与水反应生成的次氯酸具有杀菌作用,常用于自来水的消毒。在次氯酸中,氯元素的化合价为_________,氯原子容易得到电子,从而使氯元素化合价降低,因此次氯酸具有强_____________,次氯酸具有漂白作用就是基于它的这个性质。
(2)现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能是( )
A.苹果汁中的Fe2+变成Fe3+ B.苹果汁中含有Cu2+
C.苹果汁含有OH- D.苹果汁含有Na+
(3)我们在生产和生活中需要许多单质如金属铁、单质硅等。而自然界中存在的元素大多以化合态存在,把某元素由化合态变成游离态,则它( )
A.被氧化 B.被还原
C.可能被氧化,也可能被还原 D.由高价态变为零价
查看答案和解析>>
科目:高中化学 来源: 题型:
当都市里的人们陶醉在繁华的城市生活中时,是否意识到有一支“大军”正向我们逼近,影响我们的生活,危害我们的健康。
(1)在意大利,人们家里的咖啡壶大多是用回收的可乐罐制得。请再列举一种生活垃圾回收利用的事例:_________________________。
(2)回收利用垃圾,首先要对垃圾进行分类。一群环保志愿者在某社区推广垃圾分类,他们在垃圾房放置了一些有分类标识的垃圾回收箱,结果却发现仍然有许多居民并没有分类放置。造成这种现象可以排除的原因是_________________________。
A.居民嫌麻烦,没有垃圾分类的习惯 B.居民每天产生的生活垃圾量多
C.居民的环保意识不强 D.居民不清楚垃圾分类的标准
(3)下图是某居民小区中垃圾收集点(小圆圈)的布局,它在选址上存在的问题有_____________________。垃圾收集点选址应考虑的因素包括________________________。
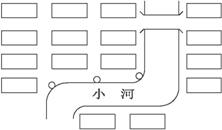
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
我们生活中的许多现象及大量物质的应用都与氧化还原反应有关。请运用氧化还原反应的知识回答下列问题。
⑴ 氯气与水反应生成的次氯酸(HClO)具有杀菌作用,常用于自来水的消毒。在次氯酸(HClO)中,氯元素的化合价为 ,氯原子容易得到电子,从而使氯元素化合价降低,因此次氯酸具有 。次氯酸具有漂白作用就是基于它的这个性质。
⑵ 氮化铝(AlN)具有耐高温、抗冲击,导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3 + N2 + 3C = 2AlN + 3CO
① 在化学方程式上标出该反应中电子转移的方向和数目。
② 在该反应中,还原剂是(写化学式) ,氧化产物是(写化学式) 。
⑶ 一个体重 50 kg的健康人,体内约有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体的吸收。
① 在人体中进行Fe2+ ![]() Fe3+的转化时,a中的Fe2+作 剂,b中的Fe3+作 剂。
Fe3+的转化时,a中的Fe2+作 剂,b中的Fe3+作 剂。
② “服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作 剂,具有 性。
③ 市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化为亚铁盐,此反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com