
【题目】下列说法错误的是( )
A. 从1 L 1 mol/L的氯化钠溶液中取出10 ml,其浓度仍是1 mol/L
B. 制成0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L(标准状况)
C. 10 g 98%硫酸(密度为1.84 g/cm3)与10 mL 18.4 mol/L硫酸的浓度是不同的
D. 0.5 L 2 mol/L的氯化钡溶液中,钡离子和氯离子总数为3×6.02×1023
【答案】C
【解析】试题分析:A.溶液是均一的,所以从1L 1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L,A正确;B.制成0.5L 10mol/L的盐酸,需要氯化氢气体的体积是0.5L×10mol/L×22.4L/mol=112L(标准状况),B正确;C.10g 98%硫酸(密度为1.84g/cm3)的浓度是![]() ,因此与10mL18.4mol/L硫酸的浓度是相同的,C错误;D.0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子的物质的量分别是0.5L×2mol/L=1mol、0.5L×2mol/L×2=2mol,所以总数为3×6.02×1023,D正确,答案选C。
,因此与10mL18.4mol/L硫酸的浓度是相同的,C错误;D.0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子的物质的量分别是0.5L×2mol/L=1mol、0.5L×2mol/L×2=2mol,所以总数为3×6.02×1023,D正确,答案选C。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】已知25 ℃时有关弱酸的电离平衡常数如下表,则下列有关说法正确的是( )
弱酸化学式 | CH3COOH | HCN | H2CO3 |
电离平衡常数(25 ℃) | 1.8×10-5 | 4.9×l0-10 | K1=4.3×10-7 K2=5.6×10-11 |
A. 等物质的量浓度的各溶液pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B. a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合后,溶液中c(Na+)>c(CN-),则a一定小于b
C. 冰醋酸中逐滴加水,则溶液的导电性、n(H+)、pH均先增大后减小
D. NaHCO3和Na2CO3混合溶液中,存在c(Na+)+c(H+)=c(OH-)+c(HCO![]() )+2c(CO
)+2c(CO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的水溶液,常温下pH值小于7的是
A.硫化钠(Na2S)B.氯化铜(CuCl2)
C.硝酸钠 (NaNO3)D.乙醇(CH3CH2OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中能大量共存的一组离子是
A.Na+、Al3+、Cl-、CO32-
B.Ca2+、Al3+、Br-、CO32-
C.K+、Ca2+、Cl-、NO3-
D.K+、NH4+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族化合物A是一种基本化工原料,可以从煤和石油中得到.A、B、C、D、E的转化关系如图所示:

已知:![]()
![]()
![]()
回答下列问题:
(1)A的化学名称是________;D中官能团名称:______;E属于_______(填“饱和烃”或“不饱和烃”).
(2)A→B的反应类型是__________,在该反应的副产物中,与B互为同分异构体的副产物的结构简式为_____________.
(3)A→C的化学方程式为______________________________________________任意一种).
(4)A与酸性KMnO4溶液反应可得到D,写出D的结构简式_____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.在加热搅拌条件下加入MgO,可除去MgCl2溶液中的Fe3+
B.40mLlmol/LCH3COONa溶液与20mLlmol/LHCl溶液混合后溶液呈酸性,所得溶液中:c (CH3COO-) > c(Cl-)>c(H+)>c(OH-)
C.常温下,Cd(0H)2和Co(0H)2的混合悬浊液中,c(Cd2+)是c(Co2+)的3.5倍
己知:Ksp[Cd(0H)2]=7.2×10-15,Ksp[Co(0H)2]=1.8×10-15
D.常温下,CH3COONa和CH3COOH的混合溶液中(pH=7): c(Na+)=c(CH3COO-)> c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学工作者发现另一种“足球分子”N60,它的结构与C60相似。下列说法中正确的是( )
A.N60和N2互为同素异形体 B.N60是一种新型化合物
C.N60和N2是同系物 D.N60和14N都是氮的同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
化学式 | AgCl | Ag2CrO4 | CH3COOH | HC1O | H2CO3 |
KSp 或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10 -5 | Ka=3.0×10-8 | Ka1=4.1×10一7 Ka =5.6×10-11 |
A.相同浓度CH3COONa和Na2CO3的混合液中,各离子浓度的关系有:
c(Na+ )>c(CO32- )>c(CH3COO一)>c(OH-)>c(H+)
B.向0.1 mol/LCH3COOH溶液中滴加NaOH溶液至溶液pH=5,此时 c(CH3COO) : c(CH3COO 一)=9 : 5
C.少量碳酸氢钠固体加入到新制的氯水中,c(HClO)增大
D.向浓度均为1×10-3mol/L的KC1和K2CrO4混合液中滴加1×10-3mol/L的AgNO3溶液,CrO42-先形成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某同学欲配制100 mL 0.10 mol·L-1的CuSO4溶液。以下操作1~5是其配制的过程及示意图:
操作1:准确称取一定质量的胆矾晶体并用适量蒸馏水溶解。
操作2:将所得溶液转移到仪器X中,用蒸馏水冲洗烧杯和玻璃棒2~3次,将洗涤液也转移到X中。
操作3:继续向X中加蒸馏水至液面离X的刻度线1~2 cm处。
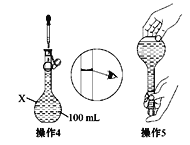
①仪器X的名称是________。称量过程中主要用到的仪器是_____________。在将烧杯中的溶液转移至容量瓶中,为了防止溶液溅出,应采取什么措施____________________。
②关于该配制过程,下列说法正确的是________。
A.操作1中,应称取胆矾晶体的质量为2.5 g
B.操作2中,洗涤液不需要转移到仪器X中
C.操作4称为定容,由于该同学的观察方法不正确,将导致所配溶液浓度偏低
D.操作5摇匀后静置,发现液面低于刻度线,应继续加水至凹液面与刻度线相切
(2)为实现金属钠在隔绝空气条件下与水反应并收集生成的气体,某研究性学习小组设计了如图发生装置。

① Y液体可以选用________。
A.煤油 B.饱和的食盐水 C.四氯化碳
②实验前检验该装置气密性的方法是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com