
【题目】![]() 中国诗词大会
中国诗词大会![]() 不仅弘扬了中华传统文化,诗句中还蕴含着许多化学知识.下列分析正确的是
不仅弘扬了中华传统文化,诗句中还蕴含着许多化学知识.下列分析正确的是![]()
A.“忽闻海上有仙山,山在虚无缥缈间”的海市蜃楼是一种自然现象,与胶体知识无关
B.“千淘万漉虽辛苦,吹尽狂沙始到金”说明金的化学性质稳定,在自然界中常以单质状态存在
C.“纷纷灿烂如星陨,霍霍喧逐似火攻.”灿烂美丽的烟花是某些金属的焰色反应,属于化学变化
D.“日照香炉生紫烟,遥看瀑布挂前川”中的“烟”是弥漫在空气中的![]() 固体颗粒
固体颗粒
科目:高中化学 来源: 题型:
【题目】中国传统文化中蕴含着丰富的化学知识。下列![]() 天工开物
天工开物![]() 的记载中不涉及合金的是
的记载中不涉及合金的是![]()
![]()
A.凡铸镜,模用灰沙,铜用锡和
B.凡倭铅![]() 锌
锌![]() 古书本无之,乃近世所立名色。其质用炉甘石
古书本无之,乃近世所立名色。其质用炉甘石![]() 主要成分为碳酸锌
主要成分为碳酸锌![]() 熬炼而成
熬炼而成
C.凡釜储水受火,日用司命系焉。铸用生铁或废铸铁器为质
D.凡治地生物,用锄、镈之属,熟铁锻成,熔化生铁淋口,入水淬健,即成刚劲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)= CO2(g)ΔH1;C(s)+ ![]() O2(g)= CO(g)ΔH2
O2(g)= CO(g)ΔH2
②S(s)+O2(g)= SO2(g)ΔH3;S(g)+O2(g)=SO2(g)ΔH4
③H2(g)+ ![]() O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
④CaCO3(s)= CaO(s)+CO2(g)ΔH7;CaO(s)+H2O(l)= Ca(OH)2(s)ΔH8
A.①B.④C.②③④D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的前四周期元素,X、Z的周期序数=族序数,由这四种元素组成的单质或化合物存在如图所示的转化关系,其中甲、戊是两常见的金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体。下列说法正确的是
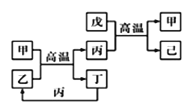
A.丙属于碱性氧化物
B.W元素在周期表中的位置是第四周期VIIIB族
C.W的原子序数是Z的两倍,金属性弱于Z
D.常温下等物质的量的甲和戊加入过量浓硝酸中,消耗的HNO3物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写和表示正确的是(△H的绝对值均正确)
A.2SO2(g)+O2(g)![]() 2SO3(g)△H=-196kJ/mol(反应热)
2SO3(g)△H=-196kJ/mol(反应热)
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol(燃烧热)
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热)
D.2NO2=O2+2NO△H=-116.2kJ/mol(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化对人类文明贡献巨大,我国古代的人民在那时候就已经广泛应用了相关的化学知识,古化文献中充分记载了古代化学研究成果。下列关于古代化学的应用和记载,对其说明不合理的是![]()
A.![]() 本草纲目
本草纲目![]() 中记载“
中记载“![]() 火药
火药![]() 乃焰消
乃焰消![]() 、硫磺、杉木炭所合,以烽燧铳机诸药者”,这是利用了“
、硫磺、杉木炭所合,以烽燧铳机诸药者”,这是利用了“![]() 的氧化性”
的氧化性”
B.李白有诗云“日照香炉生紫烟”,这是描写“碘的升华”
C.![]() 本草纲目
本草纲目![]() “烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上
“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上![]() 其清如水,味极浓烈,盖酒露也”。这里所用的“法”是指蒸馏
其清如水,味极浓烈,盖酒露也”。这里所用的“法”是指蒸馏
D.我国古代人民常用明矾水除去铜器上的铜锈![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】马日夫盐[Mn(H2PO4)2·2H2O]主要用作磷化剂;以软锰矿(主要成分为MnO2及少量的FeO、Al2O3和SiO2)为原料制备马日夫盐的主要工艺流程如图:
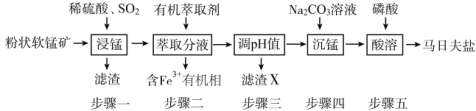
(1)按照无机物命名规律,马日夫盐[Mn(H2PO4)2·2H2O的化学名称为___。
(2)步骤一中,MnO2被SO2和___还原。若SO2气体中混有空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如图,科研人员认为Mn2+对O2与H2SO3反应起催化作用,其理由是__。

(3)滤渣X主要成分为___;步骤三调节pH时,最适宜加入的物质是__。
A.过量稀盐酸 B.适量Na2CO3溶液
C.适量磷酸溶液 D.过量CaCO3
(4)在沉锰过程中,应将Na2CO3溶液逐量加入锰盐溶液中,如果颠倒试剂混合顺序会有Mn(OH)2生成,其原因是Na2CO3溶液具有较强__性;步骤五产生马日夫盐晶体的化学反应方程式为__。
(5)Fe3+的萃取率与溶液的pH和接触时间之间的关系如图,据此分析,萃取的最佳条件为____。
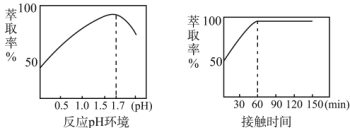
(6)马日夫盐作防锈磷化剂的原因是利用其较强的酸性以及在防锈处理过程中生成了具有保护作用的FeHPO4,马日夫盐显酸性的主要原因是__(用相关化学用语回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温下氨水中存在如下平衡:NH3H2O![]() NH4++OH-,在5份0.01mol·L-1
NH4++OH-,在5份0.01mol·L-1
的氨水中分别加入下列各物质:A、浓氨水B、纯水C、少量NaOH固体D、少量浓硫酸E、NH4Cl固体,按照要求填空:
(1)电离平衡会向逆向移动是___。
(2)c(NH4+)、c(OH-)都增大的是___,升温时氨水的Kb将___(填“增大”、“减小”或“不变”)。
(3)c(NH4+)增大,c(OH-)减小的是___。
(4)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-)。则溶液显___性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置中,K为开关,电极分别为Fe棒和C棒,电解质溶液为CuSO4溶液。
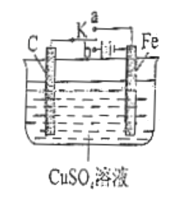
(1)当开关K置于a处时,该装置为________________(填“原电池”或 “电解池”)。写出Fe电极上的反应式____________________________。
(2)当开关K置于b处时,写出C电极上的反应式________________________。
(3)当开关K置于b处时,工作一段时间,当某电极上析出3.2g Cu时溶液的pH为____________。 (溶液的体积为1L) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com