
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA﹣ , Ⅲ代表A2﹣)所示.根据图示判断,下列说法正确的是( ) 
A.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA﹣)>c(A2﹣)>c(H+)>c(OH﹣)
B.等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水小
C.NaHA溶液中:c(OH﹣)+c(A2﹣)=c(H+)+c(H2A)
D.向上述加入20mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少
【答案】C
【解析】解:A.根据图象知,当V(NaOH)=20 mL时,发生反应为NaOH+H2A═NaHA+H2O,溶质主要为NaHA,HA﹣电离程度大于水解程度,溶液显酸性,水和HA﹣都电离出氢离子,只有HA﹣电离出A2﹣ , 所以离子浓度大小顺序是c(Na+)>c(HA﹣)>c(H+)>c(A2﹣)>c(OH﹣),故A错误;
B.等浓度的NaOH溶液与H2A溶液按体积2:1混合后,二者恰好反应生成Na2A和水,Na2A是强碱弱酸盐促进水电离,故B错误;
C.根据电荷守恒得c(OH﹣)+2c(A2﹣)+c(HA﹣)=c(H+)+c(Na+),根据物料守恒得c(Na+)=c(HA﹣)+c(H2A)+c(A2﹣),所以得c(OH﹣)+c(A2﹣)=c(H+)+c(H2A),故C正确;
D.二者恰好反应生成NaHA,此时溶液呈酸性,加水稀释显性离子浓度变小,隐性离子氢氧根离子浓度增大,所以pH增大,故D错误;
故选:C.


 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.NaHS溶液水解的方程式为:HS﹣+H2O?S2﹣+H3O+
B.向H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH﹣+18O2↑
C.在100 mL 2 mol/L FeBr2溶液中通入4.48 L氯气(标况下),充分反应:2Fe2++2Br﹣+2Cl2═2Fe3++Br2+4Cl﹣
D.用惰性电极电解饱和氯化钠溶液:2Cl﹣+2H+ ![]() H2↑+Cl2↑
H2↑+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是( )
A.共价化合物内部可能有极性键和非极性键
B.原子或离子间相互的吸引力叫化学键
C.非金属元素间只能形成共价键
D.金属元素与非金属元素的原子间只能形成离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾[KMnO4]是常用的氧化剂.工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体.中间产物为锰酸钾[K2MnO4].图1是实验室模拟制备的操作流程: 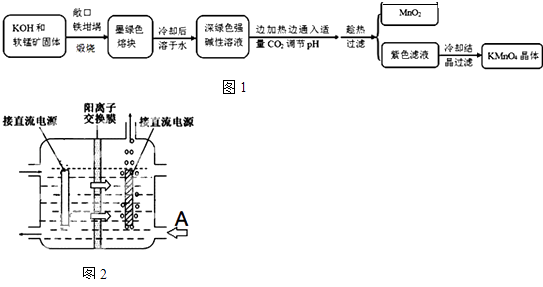
相关资料:
①物质溶解度
物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42﹣)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42﹣会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是;
(2)实验时,若CO2过量会生成KHCO3 , 导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式:;
其中氧化还原反应中氧化剂和还原剂的质量比为 .
(3)由于CO2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中 , 得到的产品纯度更高.
A.醋酸
B.浓盐酸
C.稀硫酸
(4)工业上采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图).图2中A口加入的溶液最好为 . 使用阳离子交换膜可以提高Mn元素利用率的原因为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式,正确的是( )
A.用小苏打治疗胃酸过多:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
B.AlCl3溶液中加入足量的氨水:Al3++3OH﹣═Al(OH)3↓
C.用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+
D.铝与浓氢氧化钠溶液反应:2Al+2OH﹣+2H2O═2AlO ![]() +3H2↑
+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度不是1 mol/L的是( )
A. 10 g NaOH固体溶解在水中配成250 mL溶液
B. 将80 g SO3溶于水并配成1 L的溶液
C. 将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液
D. 标况下,将22.4 L氯化氢气体溶于水配成1 L溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用.
(1)Ⅰ.脱硝:已知:H2的燃烧热为285.8kJmol﹣1
N2(g)+2O2(g)=2NO2(g)△H=+133kJmol﹣1
H2O(g)=H2O(l)△H=﹣44kJmol﹣1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为
(2)Ⅱ.脱碳:向2L密闭容器中加入2mol CO2、6mol H2 , 在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g)CH3OH(l)+H2O(l)
(I)①该反应自发进行的条件是(填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是 .
a、混合气体的平均式量保持不变 b、CO2和H2的体积分数保持不变
c、CO2和H2的转化率相等 d、混合气体的密度保持不变
e、1mol CO2生成的同时有3mol H﹣H键断裂
(II)产物甲醇可以用作燃料电池,该电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向一个电极通入空气.负极发生的电极反应式是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com