
| A. | 气体通过盛有酸性高锰酸钾溶液的洗气瓶 | |
| B. | 气体通过盛有足量溴水的洗气瓶 | |
| C. | 气体通过盛有足量蒸馏水的洗气瓶 | |
| D. | 气体与适量HCl混合 |
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙烷和乙烯 | B. | 丙烯和丙烷 | ||
| C. | 甲烷和己烷 | D. | 乙炔和乙烯基乙炔( CH2=CH-C≡CH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (R1~R4表示氢或烃基)
(R1~R4表示氢或烃基) .
. .
. (其中任一种).
(其中任一种).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
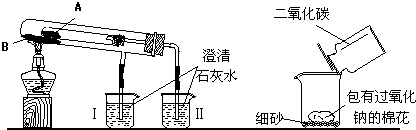
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol•L-1 | B. | 0.25mol•L-1 | C. | 0.45mol•L-1 | D. | 0.225mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将少量产品加入6mL水的试管A中,振荡,将上层液体倾析至B、C中. | 得到白色晶体和无色溶液 | |
| ② | 向试管B中加入少量BaCl2溶液. (或取试管B中溶液做焰色反应实验). | 不产生白色沉淀(或焰色不呈黄色) | 产品中不含 Na2SO4 |
| ③ | 向试管C中,加入少量FeCl3溶液(或浓溴水). | 溶液不显紫色(或无白色沉淀出现). | 产品中不含水杨酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将反应2Fe3++Fe═3Fe2+设计为原电池,则可用Zn为负极,Fe为正极,FeCl3为电解质 | |
| B. | 铜片和铝片用导线连接后插入浓硝酸中,铜作负极 | |
| C. | 镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀 | |
| D. | 铝片和镁片用导线连接后插入NaOH溶液中,Mg较活泼作负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com