
【化学——选修2:化学与技术】(15分)
过碳酸钠(2Na2CO3·3H2O2)俗称固体双氧水,是一种很好的消毒剂和供氧剂。湿法生产过碳酸钠的原理和线路如图所示(BC—1,BC—2均为稳定剂):

请回答下列问题:
(1)H2O2中添加BC—Ⅰ的目的是 ;工业纯碱中常含有微量Fe3+,加入BC—2可与Fe3+形成配合物,这样做的原因是 。
(2)过碳酸钠在高温下容易分解,所以制取时反应需控制在5℃以下进行。在反应釜中发生的主要反应为 ;常温结晶的过程中加入氯化钠、搅拌,作用是 。
(3)下列关于过碳酸钠使用和保存的说法不正确的是 。(填字母标号)
A.应与易燃或可燃物、还原剂等分开存放
B.使用时避免与眼睛、皮肤和衣服接触
C.储存于干燥洁净、不通风的仓库内
D.过碳酸钠不慎溅入眼睛应用流动清水或生理盐水冲洗,并就医
(4)过碳酸钠是一种很好的消毒剂,下列与其消毒原理相似的是 。(填字母标号)
A.乙醇 B.漂粉精 C.二氧化硫 D.过氧化钠
(5)工业上常以所含活性氧的质量分数 衡量过碳酸钠产品的优势,13%以上为优等品。取2g某厂家生产的过碳酸钠样品(所含杂质不参加反应)溶于水配成溶液,加入足量MnO2,反应完全后溶液质量减轻0.264g,则该样品中活性氧的质量分数为 。
衡量过碳酸钠产品的优势,13%以上为优等品。取2g某厂家生产的过碳酸钠样品(所含杂质不参加反应)溶于水配成溶液,加入足量MnO2,反应完全后溶液质量减轻0.264g,则该样品中活性氧的质量分数为 。
(1)增强H2O2的稳定性,防止其分解;防止Fe3+催化H2O2的分解
(2)2Na2CO3+3H2O2=2Na2CO3·3H2O2
降低过碳酸钠的溶解度,有利于过碳酸钠的析出
(3)C (4)BD (5)13.2%
【解析】
试题分析:(1)由题干可知BC—Ⅰ为稳定剂,H2O2不稳定易分解,故用BC—Ⅰ的目的为增强H2O2的稳定性,防止其分解;Fe3+可以催化H2O2分解,故加入BC—2可与Fe3+形成配合物目的防止Fe3+催化H2O2分解;过碳酸钠在高温下容易分解,所以制取时反应需控制在5℃以下进行。在反应釜中发生的主要反应为:H2O2与Na2CO3发生反应生成过碳酸钠(2Na2CO3·3H2O2),方程式为:3H2O2+2Na2CO3=2Na2CO3·3H2O2;常温结晶的过程中加入氯化钠、搅拌,作用是降低过碳酸钠的溶解度,有利于过碳酸钠析出;过碳酸钠有一定的强氧化性故A项存放正确,会腐蚀眼睛、皮肤和衣服,故B、D项正确;过碳酸钠(2Na2CO3·3H2O2)俗称固体双氧水,是一种很好的消毒剂和供氧剂,不通风的仓库内会造成仓库中氧气含量升高,发生危险,故C项错误;本题选C;(5)过碳酸钠是一种很好的消毒剂,其消毒原理为具有强氧化性能使蛋白质变性,故本题中消毒原理与其相似的有B.漂粉精、D.过氧化钠;(6)由题意可列等式关系:该样品中活性氧的质量分数=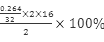 =13.2%。
=13.2%。
考点:化学与技术。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:2014-2015吉林省高一上学期期末考试化学试卷(解析版) 题型:选择题
下列有关物质分离方法的叙述中,不正确的是
A.用四氯化碳萃取碘水中的碘 B.用蒸馏的方法除去自来水中的Cl-等杂质
C.用萃取的方法分离汽油和煤油 D.用加热的方法分离氯化钠和氯化铵固体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊市高三12月月考化学试卷(解析版) 题型:选择题
下列物质转化在给定条件下不能实现的是
①SiO2 Na2SiO3
Na2SiO3 H2SiO3
H2SiO3
②S SO3
SO3 H2SO4
H2SO4
③饱和NaCl(aq) NaHCO3
NaHCO3 Na2CO3
Na2CO3
④Fe2O3 FeCl3(aq)
FeCl3(aq)  无水FeCl3
无水FeCl3
⑤MgO MgCl2溶液
MgCl2溶液 Mg
Mg
A.①③⑤ B.②③④ C.②④⑤ D.①④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期末考试化学试卷(解析版) 题型:选择题
X、Y、Z、W有如图所示的转化关系,则X、Y可能是
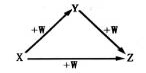
①C、CO ②AlCl3 Al(OH)3 ③N2、NO ④S、SO2
A.②③ B.①② C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期末考试化学试卷(解析版) 题型:选择题
下列物质的分类依据正确的是
物质类别 | 分类依据 | |
A | 酸 | 电离时能否产生氢离子 |
B | 碱性氧化物 | 是否属于金属氧化物 |
C | 胶体 | 能否发生丁达尔现象 |
D | 强电解质 | 水溶液中能否完全电离 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省新余市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
N2(g)+3H2(g)≒2NH3(g) △H=-92.2KJ/mol。在2L恒容密闭容器中各物质的浓度随时间变化的曲线如图所示。下列说法错误的是

A.若时段I中投入物质的浓度为原来的2倍,则反应物的转化率增大,平衡常数不变
B.第25min改变的条件是将NH3从反应体系中分离出去
C.若第60min时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度
D.前25min内反应放出的热量为46.lkJ
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南通市高三第一次模拟化学试卷(解析版) 题型:填空题
(14分)氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)某课外学习小组欲制备少量NO气体,写出铁粉与足量稀硝酸反应制备NO的离子方程式: 。
(2)LiFePO4是一种新型动力锂电池的电极材料。
①下图为某LiFePO4电池充、放电时正极局部放大示意图,写出该电池放电时正极反应方程式: 。

②将LiOH、FePO4·2H2O(米白色固体)与还原剂葡萄糖按一定计量数混合,在N2中高温焙烧可制得锂电池正极材料LiFePO4。焙烧过程中N2的作用是 ;实验室中以Fe3+为原料制得的FePO4·2H2O有时显红褐色,FePO4·2H2O中混有的杂质可能为 。
(3)磷及部分重要化合物的相互转化如图所示。

①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是 。
②不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为 。
③步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南通市高三第一次模拟化学试卷(解析版) 题型:选择题
25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.pH=1的无色溶液中:Na+、Cu2+、Cl-、CO32-
B.使酚酞呈红色的溶液中:K+、Na+、NO3-、Cl-
C.0.1 mol/L的FeCl2溶液中:H+、Al3+、SO42-、ClO-
D.由水电离出的c(H+)=1×10-10mol/L的溶液中:Mg2+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市八校高三第二次联考化学试卷(解析版) 题型:选择题
下列事实说明HNO2为弱电解质的是
①0.1 mol/L HNO2溶液的pH=2.1; ②常温下NaNO2溶液的pH>7 ;
③用HNO2溶液做导电实验时,灯泡很暗; ④HNO2溶液和KCl溶液不发生反应
⑤HNO2能与碳酸钠反应制CO2; ⑥HNO2不稳定,易分解
A.①②③⑤ B.①②④⑤ C.①②⑥ D.①②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com