
| A、① | B、①④ | C、③④ | D、①③ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
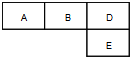 有M、A、B、D、N、E六种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在右表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:
有M、A、B、D、N、E六种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在右表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答: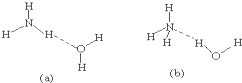
查看答案和解析>>
科目:高中化学 来源: 题型:
 和
和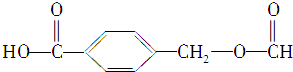 若各1mol该有机物在一定条件下与NaOH溶液反应,消耗NaOH的物质的量分别是( )
若各1mol该有机物在一定条件下与NaOH溶液反应,消耗NaOH的物质的量分别是( )| A、3 mol、2 mol |
| B、2 mol、2 mol |
| C、3 mol、3 mol |
| D、5 mol、3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 |
| B、侯氏制碱法的工艺过程中应用了物质溶解度的差异 |
| C、碘是人体必须微量元素,所以要多多吃富含高碘酸的食物 |
| D、氯化铝是一种电解质,可用于电解法制铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状态下,22.4LC4H6中含有碳碳叁键数一定为NA |
| B、含1molFeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目为NA |
| C、在标准状况下,22.4L辛烷中所含分子数为NA |
| D、106 g Na2CO3固体中的阴离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S2C12晶体中不存在离子键 |
| B、S2C12分子中各原子均达到8电子稳定结构 |
| C、S2C12在熔融状态下能导电 |
| D、S2C12与水反应后生成的气体难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②中由水电离出的c(H+)=1×10-12mol/L |
| B、将①、③混合,若有pH=7,则消耗溶液的体积:③>① |
| C、将②、④等体积混合(体积变化忽略不计),则c(CH3COO-)+c(CH3COOH)=0.01 mol/L |
| D、将四份溶液均稀释10倍以后的溶液pH:③>④,②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
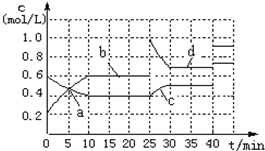
| A、a、b、c、d四个点中处于平衡状态的点是a、b |
| B、反应进行至25min时,曲线发生变化的原因是加入了 0.4molN |
| C、若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
| D、若40min后出现如图所示变化,则可能是加入了某种催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com