
A、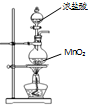 用装置制取氯气 |
B、 用装置除去氯气中的少量氯化氢和水蒸气 |
C、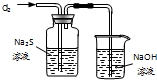 用装置可证明Cl2的氧化性强于S |
D、 用装置可以完成“喷泉”实验 |


 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
| A、不能与金属钠发生反应 |
| B、能发生取代反应 |
| C、能溶于水,不溶于乙醇 |
| D、符合通式CnH2nO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的溶液中:Na+、NH4+、NO3-、ClO- | ||
B、
| ||
| C、0.1 mol?L-1NaAlO2溶液中:Na+、Al3+、HCO3-、SO42- | ||
| D、常温下,在c(H+)水?c(OH-)水=10-26的溶液中:K+、Fe2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲 | 乙 | 丙 | |
| 丁 | 戊 | ||
| 己 |
| A、乙、戊、庚三种元素形成的化合物只含共价键 |
| B、原子半径:甲>乙>丙 |
| C、最高价氧化物对应水化物的酸性:戊>丁>己 |
| D、丁与己的原子序数相差8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验事实 | 结论 | |
| ① | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | NaHCO3溶液与Na[Al(OH)4]溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| ④ | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色晶体加入氢氧化钠浓溶液中并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该晶体中一定有NH4+ |
| A、②③⑤ | B、①②③ |
| C、③④⑤ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
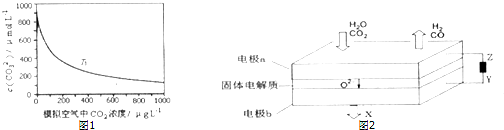
| ||
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“风雨雷电”和“雾霾”都属于自然现象 |
| B、地下钢管连接锌块是采用牺牲阳极的阴极保护法 |
| C、乳酸分子中既有羟基又有羧基,因此可在一定条件下缩聚得到聚乳酸(PLA).该高分子化合物是一种可降解的环保材料 |
| D、手机外壳上贴的碳纤维外膜是一种新型无机高分子材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com