
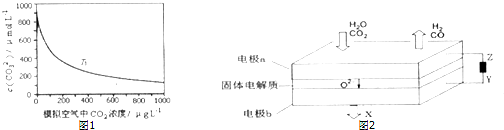
| ||
| 高温 |
| c2(CO)?c2(H2) |
| c(CO2)?c(CH4) |
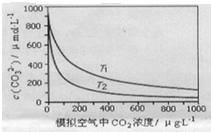 ;
; ;
;| 3-x |
| 3-x+3-x+2x+2x |
| c2(CO)?c2(H2) |
| c(CO2)?c(CH4) |
| 42×42 |
| 1×1 |


科目:高中化学 来源: 题型:

| A、SiO2与干冰的晶体结构相似 |
| B、SiO2耐腐蚀,不与任何酸反应 |
| C、工业上用SiO2制备粗硅 |
| D、光纤主要成分是SiO2,具有导电性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、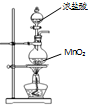 用装置制取氯气 |
B、 用装置除去氯气中的少量氯化氢和水蒸气 |
C、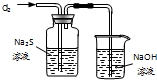 用装置可证明Cl2的氧化性强于S |
D、 用装置可以完成“喷泉”实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑤ | B、②③ | C、①④ | D、③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )| A、2.1mL | B、2.4mL |
| C、3.6mL | D、4mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C3H4和C2H6 |
| B、C3H6和C4H8O |
| C、C3H6O2和C3H8O |
| D、C3H8O和C4H6O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、其浓溶液如果不慎沾在皮肤上,应立即用酒精擦洗 |
| B、其水溶液显强酸性,俗称石炭酸 |
| C、超过65℃可以与水以任意比互溶 |
| D、纯净的苯酚是无色晶体,在空气中易被氧化而呈粉红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应中旧键断裂需吸收能量,新键形成需放出能量,所以总能量不变 |
| B、上述热化学方程式中的△H的值与反应物的用量无关 |
| C、该反应的化学能可以转化为电能 |
| D、反应物的总能量高于生成物的总能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com