
 4NO2 (g)+ O2(g) ΔH > 0;T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2 (g)+ O2(g) ΔH > 0;T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:| 时间/s | 0 | 500 | 100 0 | 150 0 |
| c(N2O5)/ mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
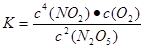 。解得2X=2.5mol/L.因此平衡时N2O5的转化率为50%。正确。D. 达平衡后其他条件不变,将容器的体积压缩到原来的1/2,即增大了压强,假如平衡不发生移动,c(N2O5)是原来的2倍,也就是5.00 mol/L.而增大压强,化学平衡逆向移动,c(N2O5)增大,所以c(N2O5)> 5.00 mol/L.正确。
。解得2X=2.5mol/L.因此平衡时N2O5的转化率为50%。正确。D. 达平衡后其他条件不变,将容器的体积压缩到原来的1/2,即增大了压强,假如平衡不发生移动,c(N2O5)是原来的2倍,也就是5.00 mol/L.而增大压强,化学平衡逆向移动,c(N2O5)增大,所以c(N2O5)> 5.00 mol/L.正确。

科目:高中化学 来源:不详 题型:单选题
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ |
| C.反应至4 min时,若HCl的浓度为0.12 mol·L-1,则H2的反应速率为0.03 mol·L-1·min-1 |
| D.当反应吸收热量为0.025 Q kJ时,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液恰好反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
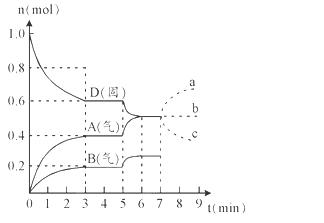
 2A(g) + B(g)该反应的平衡常数表达式为K=c(A)2·c(B)
2A(g) + B(g)该反应的平衡常数表达式为K=c(A)2·c(B)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g);ΔH<0,下列研究目的和示意图相符的是 ( )。
2NH3(g);ΔH<0,下列研究目的和示意图相符的是 ( )。| | A | B | ||
| 研究 目的 | 压强对反应的影 响(p2>p1) | 温度对反应的影响 | ||
| 图示 |  | 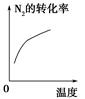 | ||
| | C | D | | |
| 研究 目的 | 平衡体系增加N2 对反应的影响 | 催化剂对反应的影响 | | |
| 图示 | 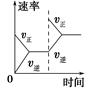 | 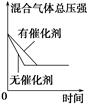 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

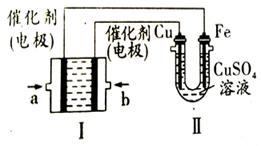
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
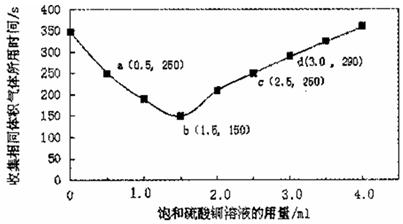
| A.饱和硫酸铜溶液用量过多不利于更快收集氢气 |
| B.a ,c两点对应的氢气生成速率相等 |
| C.b点对应的反应速率为v( H2SO4)=1.0x10-3mol·L -1 ·s-1 |
| D.d点没有构成原电池,反应速率减慢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)。在相同时间内表示该反应速率最快的是
2NH3(g)。在相同时间内表示该反应速率最快的是| A.v(H2)=0.1 mol/(L·s) | B.v(N2)=0.1 mol/(L·s) |
| C.v(N2)=0.2 mol/(L·s) | D.v(NH3)=0.3 mol/(L·s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com