
【题目】下列离子方程式正确的是( )
A.向氨水中滴入盐酸:OH﹣+H+=H2O
B.石灰乳与Na2CO3溶液反应:Ca2++CO32﹣=CaCO3↓
C.向澄清石灰水中通入少量二氧化碳:Ca2++2OH﹣+CO2=CaCO3↓+H2O
D.向沸水中逐滴滴加FeCl3饱和溶液:Fe3++3H2O ![]() Fe(OH)3↓+3 H+
Fe(OH)3↓+3 H+
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
【题目】关于铝的性质和用途的下列叙述,错误的是( )
A.铝可作导线和电缆
B.铝箔可以作食品、饮料的包装
C.铝制容器可用来盛装冷的浓硫酸
D.铝的硬度很大,可用作制造汽车、船舶、飞机等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的四种溶液中加入以下各种离子,能在原溶液中大量共存的是
A. 常温下强酸性 的溶液: K+、HCO3-、Br、Ba2+
B. 滴加酚酞溶液显红色的溶液:Fe3+、NH4+、Cl、NO3-
C. 所含溶质为FeCl3的溶液:K+、SO42-、NO3-、H+
D. 强碱性溶液:Cu2+、Na+、Mg2+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生活密切相关,下列说法正确的是
A.“歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料
B.工业上通常用电解Na、Mg、Al对应的氯化物制取该三种金属单质
C.Fe3O4俗称铁红,常做红色油漆和涂料
D.燃料电池的燃料都在负极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:

查阅资料:Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。(Sn: 119)
回答下列问题:
(1) 操作Ⅰ是________、过滤洗涤。
(2)SnCl2粉末需加浓盐酸进行溶解,目的是_______________________________。
(3)加入Sn粉的作用有两个:①调节溶液pH,②____________________________。[
(4)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是___________________。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl![]() SnCl2+ H2↑;
SnCl2+ H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2+ K2Cr2O7+ 14HCl![]() 6FeCl3+ 2KCl + 2CrCl3+7H2O
6FeCl3+ 2KCl + 2CrCl3+7H2O
现取0.80 g锡粉,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液20.00mL。则锡粉中锡的纯度为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制0.5mol/L的NaOH溶液225mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却⑨摇动,其正确的操作顺序为 . 本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、 .
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,则烧杯的实际质量为g,要完成本实验该同学应称出g NaOH. 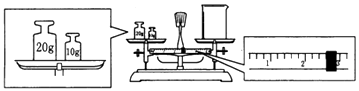
(3)使用容量瓶前必须进行的一步操作是 .
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是 . (填写序号)
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③定容时俯视刻度线
④容量瓶不干燥,含有少量蒸馏水
⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有Ba2+ , Mg2+ , Ag+ , 现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图(已知溶液2为无色溶液) 
(1)沉淀的化学式:沉淀1: , 沉淀2:;沉淀3: .
(2)写出“混合液+A”的离子方程式:;“生成沉淀2”的离子方程式 .
(3)从溶液1和B反应后分离得到沉淀2和溶液2的实验中,使用到的玻璃仪器有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃时,用蒸馏水稀释1 mol·L-1的醋酸溶液至0.01 mol·L-1,随着溶液的稀释,下列各项中始终保持增大趋势的是( )
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com