
����Ŀ����һ���¶��£���X��Y ��0.16 mol����10 L �����ܱ������У�������Ӧ��2X(g)+ Y(s)![]() 2Z(g) ��H < 0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±�����˵����ȷ����( )
2Z(g) ��H < 0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±�����˵����ȷ����( )
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.10 | 0.09 | 0.09 |
A����Ӧǰ2min��ƽ������v(Z)=2.0��10-3 mol/(L��min)
B�������������䣬����һ������Y����Ӧ����һ���ӿ�
C����Ӧ����4sʱ��X��ת����75%
D����Ӧ�ﵽƽ��ʱ��X�����ʵ���Ũ��Ϊ0.02mol��L-1
���𰸡�C
��������
���������A��2min��Y���ʵ����仯Ϊ0.16mol-0.12mol=0.04mol����Z�ı仯�����ʵ���Ϊ0.08mol������v=![]() =
=![]() =4.0��10-3 mol/(Ls)����A����B������Ӱ�����ʵ����أ�Y���壬��������Ũ�Ȳ��䣬���Բ�Ӱ�췴Ӧ���ʣ���B����C����Ӧ����4sʱ��Y��ת�������ʵ���Ϊ0.16mol-0.10mol=0.06mol�������X��ת�������ʵ���Ϊ0.06mol��2=0.12mol���ٸ���ת����=
=4.0��10-3 mol/(Ls)����A����B������Ӱ�����ʵ����أ�Y���壬��������Ũ�Ȳ��䣬���Բ�Ӱ�췴Ӧ���ʣ���B����C����Ӧ����4sʱ��Y��ת�������ʵ���Ϊ0.16mol-0.10mol=0.06mol�������X��ת�������ʵ���Ϊ0.06mol��2=0.12mol���ٸ���ת����=![]() ��100%�����X��ת����Ϊ
��100%�����X��ת����Ϊ![]() ��100%=75%����C��ȷ��D����Ӧ�ﵽƽ��ʱ��Yת�������ʵ���Ϊ0.16mol-0.09mol=0.07mol����X��ת�������ʵ���Ϊ0.07mol��2=0.14mol������ƽ��ʱX�����ʵ���Ϊ0.6mol-0.14mol=0.02mol������c=
��100%=75%����C��ȷ��D����Ӧ�ﵽƽ��ʱ��Yת�������ʵ���Ϊ0.16mol-0.09mol=0.07mol����X��ת�������ʵ���Ϊ0.07mol��2=0.14mol������ƽ��ʱX�����ʵ���Ϊ0.6mol-0.14mol=0.02mol������c=![]() ���X�����ʵ���Ũ��Ϊ
���X�����ʵ���Ũ��Ϊ![]() =0.002molL-1����D����ѡC��
=0.002molL-1����D����ѡC��


 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D���ֽ������±���װ�ý���ʵ�顣
װ�� |
|
|
|
���� | ���۽���A�����ܽ� | C���������� | A����������� |
����ʵ������ش��������⣺
��1��װ�ü��и����ĵ缫��Ӧʽ��__��
��2��װ�����������ĵ缫��Ӧʽ��__��
��3��װ�ñ�����Һ��pH__����������С�����䡱����
��4�����ֽ�����������ǿ������˳����__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ����ȡ��̽���������ʣ�������װ��(���ּг�װ������ȥ)����ʵ�顣[��ȡ�����ķ�Ӧԭ����2NH4Cl+Ca(OH)2=CaCl2+2NH3��+2H2O]

��ʵ��̽����
(1)��������ԭ����ʵ������ȡ����Ӧѡ����ͼ�� ����װ�ý���ʵ�顣
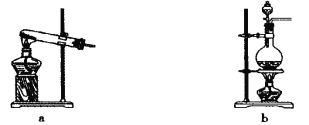
(2)Bװ���еĸ������ѡ�� (���ʯ�ҡ���Ũ���ᡱ)��
(3)��5.35 g NH4Cl����������Ca(OH)2��Ӧ�������Ƶñ�״���°��������Ϊ L��(NH4Cl��Ħ������Ϊ53.5 g��mol��1)
(4)����ͨ��C��Dװ��ʱ����ֽ��ɫ�ᷢ���仯���� (�C����D��)��
(5)��ʵ�����һ��ʱ���ѹEװ���еĽ�ͷ�ιܣ�����1��2��Ũ���ᣬ�ɹ۲쵽�������� ��
(6)Fװ���е���©�������� ��
����չӦ�á�
(7)ijͬѧ�ð����͵μӷ�̪��ˮ����Ȫʵ�飬������ƿ�ڲ�����ɫ��Ȫ������˵���������� ����(�����)��
a����ԭ�� b����������ˮ c����ˮ��Ӧ���ɼ�������
(8)��������;�ܹ㡣����ð����������������� 8NH3 + 6NO2 =7N2 + 12H2O
�÷�Ӧ�а������� (������ԡ���ԭ�ԡ�)��
�����оٳ���������һ����; ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г����ʵIJ����в���ȷ����
A. �����л������ۣ���������ռ���Һ��ַ�Ӧ�����
B. FeCl2��Һ�л���FeCl3����������۳�ַ�Ӧ�����
C. Na2CO3�����л�������NaHCO3:��������NaOH��Һ
D. AI(OH)3�л���Mg(OH)2:���������ռ���Һ����ˣ�����Һ��ͨ�����CO2�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��
CO(g)+H2O(g)![]() CO2(g)+H2(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO2(g)+H2(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�ش��������⣺
(1) �÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=__________,�÷�ӦΪ_________��Ӧ(�����Ȼ����)��
���ı�����ʹƽ��������Ӧ�����ƶ�����ƽ�ⳣ��_____________(�����)
��һ������ ��һ����С ���������� ������С��������п���
(2) ���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������_______________
a.������ѹǿ���� b.���������c(CO)����
c.v��(H2)=v��(H2O) d.c(CO)=c(CO2)
(3) ����ͬ����CO (g) ��H2O (g) �ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������У����з�Ӧ CO (g) �� H2O (g) ![]() CO2 (g) �� H2 (g)���õ���������������
CO2 (g) �� H2 (g)���õ���������������
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min[ | ||
H2O | CO | CO2 | CO | |||
A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
C | 900 | a | b | c | d | t |
��ͨ�������֪��CO��ת����ʵ��A ʵ��B(������������������������С����)���÷�Ӧ������ӦΪ (����������������)�ȷ�Ӧ��
����ʵ��CҪ�ﵽ��ʵ��B��ͬ��ƽ��״̬����a��bӦ����Ĺ�ϵ�� (�ú�a��b����ѧʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�ɢϵ���ܷ��������ЧӦ���ǣ�������
A. ���� B. ţ�� C. ������Һ D. �̡��ơ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.NH3��CO2��ˮ��Һ�����磬����NH3��CO2���ǵ����
B. ���ǡ��ƾ���ˮ��Һ���ۻ�ʱ�������磬���������Ƿǵ����
C.ͭ��ʯī�����磬���������ǵ����
D.Һ̬HCl����̬NaCl�������磬����HCl��NaCl�����ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ���֪A��B��E ����ԭ������㹲��10�����ӣ�����3��Ԫ�ص�����������ˮ�����������ܷ�����Ӧ�����κ�ˮ��CԪ�ص������������ȴ�����������4��DԪ��ԭ�Ӵ�����������������������3��
��1��д����Ӧ��Ԫ�ط��ţ�C________��D_______
��2���õ���ʽ��ʾA��E��Ԫ���γɻ�����Ĺ��̣�___________________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I����һ��2L���ܱ������У�������Ӧ2SO3��g��![]() 2SO2��g��+O2��g������H��0������SO3�ı仯��ͼ��ʾ��
2SO2��g��+O2��g������H��0������SO3�ı仯��ͼ��ʾ��
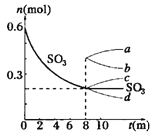
��1����O2��ʾ0��8min�ڸ÷�Ӧ��ƽ������v=__________��
��2�������¶ȣ� Kֵ��__________�������������ƽ����Է���������__________������������������С��������������
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����__________
a��v��SO3��=2v��O2�� b��������ѹǿ���ֲ���
c��v����SO2��=2v����O2�� d���������ܶȱ��ֲ���
��4����8min��ѹ������Ϊ1L����SO3�ı仯����Ϊ__________
A�� a B�� b C�� c D�� d��
II��������A��B�����ݻ�Ϊ2L���ܱ��������������·�Ӧ��4A��g��+B��g��=2C��g����ʼʱ����0.5molB��һ������A����Ӧ���е�4sĩ�����v��B��=0.0125mol��L-1��s-1��A��C��Ϊ0.2mol����
��1��V��A�� =____________
��2����ӦǰA��_________mol
��3��B��ת����Ϊ____________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com