
���и���˵���У�����ȷ���� �� ��
| A����������ˮͨ��SO2����ʱ��pH��SO2���ʵ����Ĺ�ϵͼ |
| B��������c(H+)��ͬ�Ĵ�����������ˮʱ��c(H+)��ˮ����Ĺ�ϵͼ |
| C�����³�ѹ�£���2b mol CO2����ͨ��1L bmol��L-1��NaOH��Һ�У�����CO2�����ͨ�룬��Һ����ˮ�������c��H���������ͼ�仯��ϵ |
| D������������Һ�еμ�ϡ����õ���pH��5�Ļ����Һ�У�c(Na��)��c(NO3��) |
D
�������������A����ˮ���������Ӧ�����廯������ᣬpH���ͣ�A��ȷ��B��������ǿ�ᣬ���������ᣬ���ڵ���ƽ�⣬ϡ�ʹٽ����룬����ϡ����ͬ�ı���ʱ�����pH�仯��B��ȷ��C��������̼���������Ʒ�Ӧ����̼���ƣ�������̼����������̼�����ơ�����������ϵ��֪�����յõ�����̼�����ƺ�̼��Ļ��Һ������������ǿ�����ˮ�ĵ��룬��̼���ơ�̼�����ƾ�ˮ��ٽ�ˮ�ĵ��룬��̼�����Ƶ�ˮ��̶�С��̼���Ƶ�ˮ��̶ȣ����ͼ���ϣ�C����ȷ��D������������Һ�еμ�ϡ����õ���pH��5�Ļ����Һ�и��ݵ���غ��֪c(Na��)+ c(H��)��c(OH��)+ c(Cl��)+��c(NO3��)��c(H��)��c(Cl��)��������Һ�У�c(Na��)��c(NO3��)��D��ȷ����ѡD��
���㣺����������ʵĵ��롢����ˮ���Լ���Һ������Ũ�ȴ�С�Ƚ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪PbI2��Ksp=7.0��10-9����7.5��10-3 mol/L��KI��ijŨ�ȵ�Pb��NO3��2��Һ�������Ϊ2��1��ϣ�������PbI2��������Pb��NO3��2��Һ����СŨ��Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��������ˮ�����г�����ɱ��������HClO��ɱ��������ClO��ǿ��25��ʱ����-��ˮ��ϵ�д�������ƽ���ϵ��
Cl2(g)  Cl2(aq) K1=10��1.2
Cl2(aq) K1=10��1.2
Cl2(aq)+ H2O  HClO + H+ +Cl�� K2=10��3.4
HClO + H+ +Cl�� K2=10��3.4
HClO  H+ + ClO�� Ka=?
H+ + ClO�� Ka=?
����Cl2(aq)��HClO��ClO���ֱ�����������ռ����(��)��pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�����ȷ����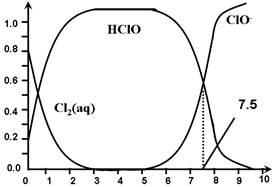
A��Cl2(g)+ H2O  2H+ + ClO�� + Cl�� K=10��10.9 2H+ + ClO�� + Cl�� K=10��10.9 |
| B�����ȴ���ˮ��ϵ�У�c(HClO) + c(ClO��) =c(H+)��c(OH��) |
| C�����ȴ�������ˮʱ��pH=7.5ʱɱ��Ч����pH=6.5ʱ�� |
| D���ȴ�������ˮʱ�����ļ���ɱ��Ч�����ڶ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵����ȷ����
| A�������£�PH=9��̼������Һ����ˮ�������c(OH��)=1��10-9mol��L-1 |
| B���¶���ͬʱ����������Һ��ǿ��ϡ��Һ�У�ˮ�����ӻ�����Kw��ͬ |
| C����pH��4�Ĵ�����Һϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ����� |
| D���к͵����pH��ͬ��H2SO4��HCl��Һ������NaOH�����ʵ���Ϊ2:1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����ʵ���ܴﵽԤ��Ŀ�ĵ��� �� ��
| ��� | ʵ������ | ʵ��Ŀ�� |
| A | �����£���pH��ֽ�ֱ�ⶨŨ��Ϊ0.1mol��L��1NaClO��Һ��0.1mol��L��1CH3COONa��Һ��pH | �Ƚ�HClO��CH3COOH������ǿ�� |
| B | ���з�̪��Na2CO3��Һ�м�������BaC12���壬��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
| C | ��10mL 0.2 mol/L NaOH��Һ�е���2��0.1 mol/L MgCl2��Һ��������ɫ�������ٵμ�2��0.1 mol/LFeCl3��Һ�������ɺ��ɫ���� | ֤������ͬ�¶��µ�Ksp�� Mg(OH)2 ��Fe(OH)3 |
| D | �ֱ�ⶨ�����µ����ʵ���Ũ�ȵ�Na2SO3��Na2CO3��Һ��pH�����߽ϴ� | ֤���ǽ�����S��C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪25��ʱ�����볣��Ka(HF)��3.6��10-4���ܶȻ�����Ksp(CaF2)��1.46��10-10������1 L 0.2mol��L-1HF��Һ�м���1 L 0.2 mol��L-1CaCl2��Һ��������˵���У���ȷ���ǣ� ��
| A��25��ʱ��0.1 mol��L-1HF��Һ��pH��1 | B��Ksp(CaF2)���¶Ⱥ�Ũ�ȵı仯���仯 |
| C������ϵ����CaF2�������� | D������CaCl2��Һ����ϵ�е�c(H+)Ũ�Ȳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����������ȷ����
| A��FeCl3��Һ�м���þ�������ݲ��� |
| B��C12��SO2����ʹƷ����Һ��ɫ��˵�����߾���Ư���� |
| C��Ǧ�����ڷŵ�����У�����������С�������������� |
| D����NaC1��Һ����ͨ������CO2����ͨ������NH3��������NaHCO3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£���20mL 0.2mol/L H2A��Һ�еμ�0.2 mol/L NaOH��Һ���й��������ʵ����仯��ͼ������I����H2A��II����HA����III����A2�����������ʾ����NaOH�������������ͼʾ�жϣ�����˵����ȷ����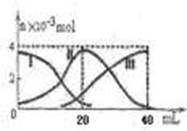
| A����V(NaOH)=40mLʱ��c (Na+)+ c(H+)="2" c(A2��)+c(OH��) |
| B����V(NaOH)=20mLʱ����Һ������Ũ�ȴ�С��ϵ��c(Na+)>c(HA��)>c(H+)>c(A2��)>c(OH��) |
| C���μӹ����е���Һ������ʱ��V(NaOH)<20mL |
| D��HA���ĵ���̶�С��ˮ��̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����Ƕ�Ԫ���ᣬ���������Һ�����ԡ���0.1mol��L��1 KHC2O4��Һ�У����й�ϵ��ȷ����
| A��c(K+)+c(H+) = c(HC2O4��)+c(OH��)+c(C2O42��) |
| B��c(HC2O4��)+c(C2O42��) =" 0.1" mol��L��1 |
| C��c(C2O42��) < c(H2C2O4) |
| D��c(K+) = c(H2C2O4)+c(HC2O4��)+c(C2O42��) |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com