
| A. | 还原剂是HCl,氧化剂是MnO2 | |
| B. | 每消耗1mol MnO2,转移电子的物质的量为2 mol | |
| C. | 每转移1mol电子,则可以制得标况下Cl2 22.4L | |
| D. | 生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质 |
分析 MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑中,Mn元素的化合价降低,Cl元素的化合价升高,以此来解答.
解答 解:A.Mn元素的化合价降低,Cl元素的化合价升高,还原剂是HCl,氧化剂是MnO2,故A正确;
B.每生成1molCl2,转移电子的物质的量为1mol×2×(1-0)=2mol,故B正确;
C.每消耗1molMnO2,得到2mol电子,生成1mol的氯气,所以每转移1mol电子,则可以制得标况下Cl2 11.2L,故C错误;
D.盐酸易挥发,则生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质,故D正确;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Al2O3用来制造耐高温的实验仪器 | |
| B. | Fe2O3常用作油漆和涂料 | |
| C. | 过氧化钠可以用作供氧剂、漂白剂等 | |
| D. | 熟石灰常直接用来治疗胃酸过多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗硅是由焦炭和二氧化硅在电炉中反应制得 | |
| B. | 硅的化学性质不活泼,常温下只与F2、HF、强碱反应 | |
| C. | 单质硅的主要用途为制造半导体材料和硅合金的原料 | |
| D. | SiO2制成的玻璃纤维,由于电能力强而被用于制造光缆 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
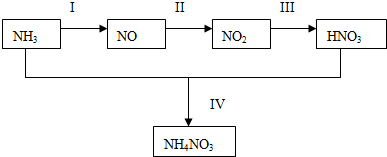
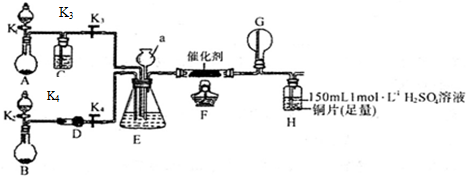
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol | |
| B. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则稀醋酸与稀NaOH溶液反应生成1 mol 水,放出57.3kJ热量 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
B | 17.9 | 290 | 1.26 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同 | |
| B. | 胶粒能透过滤纸,但不能透过半透膜 | |
| C. | 胶体与其他分散系的本质区别是丁达尔效应 | |
| D. | Al(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=12的溶液中,K+、Cl-、AlO2-、NH4+可以大量共存 | |
| B. | 由0.1 mol•L-1一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H2O?HA+OH- | |
| C. | 由0.1 mol•L-1一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=B++OH- | |
| D. | 在pH=0的溶液中,Na+、NO3-、SO32-、K+可以大量共存 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com