
1.化学与生活密切相关,下列说法正确的是( )
A. 二氧化硫可广泛用于食品的漂白
B. 煤经过气化和液化等物理变化可以转化为清洁燃料
C. 淀粉、油脂和蛋白质都是天然高分子化合物,都能发生水解反应
D. 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程
考点: 二氧化硫的化学性质;油脂的性质、组成与结构;淀粉的性质和用途.
专题: 化学应用.
分析: A.二氧化硫对人体有害,不能用于漂白食品;
B.煤的气化和液化为化学变化;
C.油脂不是高分子化合物;
D.淀粉可水解生成葡萄糖,葡萄糖在酒曲酶的作用下可生成乙醇.
解答: 解:A.二氧化硫对人体有害,不能用于漂白食品,只能用于工业漂白,故A错误;
B.煤的气化为碳和水反应生成水煤气的过程,液化为为碳和水反应生成甲醇的过程,都化学变化,故B错误;
C.油脂相对分子质量较小,不是高分子化合物,故C错误;
D.淀粉可水解生成葡萄糖,葡萄糖在酒曲酶的作用下可生成乙醇,故D正确.
故选D.
点评: 本题考查较为综合,涉及二氧化硫的性质和用途、煤的综合运用、高分子化合物以及淀粉的性质和用途,为高考常见题型,侧重于基础知识的考查,有利于培养学生的良好的科学素养和提高学习的积极性,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:
小牧家里收藏了一件清代的铝制佛像,该佛像至今仍保存十分完好。该佛像未锈蚀的主要原因是
A.铝的化学性质非常稳定,不易发生化学反应 B.铝的氧化物容易发生还原反应
C.铝被氧化生成一层致密的氧化膜薄膜 D.铝的氧化物熔点很高
查看答案和解析>>
科目:高中化学 来源: 题型:
化学是一门以实验为基础的科学,化学实验是化学学习的重要内容。
(1)根据你掌握的知识,下列描述正确的是 (填序号)
①将0.2mo1·L-1FeC13溶液滴加沸水中,然后继续加热并不断搅拌可制得氢氧化铁胶体;
②将95g蒸馏水倒入盛有5g氯化钠的200ml的烧杯中,搅拌溶解,配制5%的食盐水;
③实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉
④使用容量瓶,滴定管、分液漏斗时,首先应检验仪器是否漏水;
⑤向某溶液中加入Ba(NO3)2溶液有白色沉淀产生,加盐酸沉淀不消失,则原溶液中一定含有SO42-。
(2)实验室中需要480ml0.4mo1·L-1CuSO4溶液,应称取硫酸铜晶体(CuSO4·5H2O)的质量是 g;所用仪器除托盘天平(带砝码)、量筒、烧杯、玻璃棒、药匙外,还缺少的玻璃仪器是 ;在观察液面定容时,若俯视刻度线,会使所配制的溶液的浓度 ;(填“偏高、偏低或无影响”下同) 转移溶液前容量瓶内有少量蒸馏水 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
A+B→X+Y+ H2O(为配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,该反应的化学方程式是 .
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是 .
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中.
①A元素在周期表中的位置是______ (填所在周期和族);Y的化学式是______.
②含a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是______ mol.
(4)若A、B、X、Y均为化合物.A溶于水电离出的阳离子和水作用的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色.则向A中逐滴加入B的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3 主要:Cu2++CO32─+H2O═Cu(OH)2↓+CO2↑
次要:Cu2++CO32─═CuCO3↓
(2)CuSO4+Na2S 主要:Cu2++S2─═CuS↓
次要:Cu2++S2─+2H2O═Cu(OH)2↓+H2S↑
则下列几种物质的溶解度大小的比较中,正确的是( )
|
| A. | CuS<Cu(OH)2<CuCO3 | B. | CuS>Cu(OH)2>CuCO3 | C. | Cu(OH)2>CuCO3>CuS | D. | Cu(OH)2<CuCO3<CuS |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验可行的是( )
|
| A. | 用澄清石灰水检验CO中含有的CO2 |
|
| B. | 用BaCl2除去NaOH溶液中混有的少量Na2SO4 |
|
| C. | 用KSCN溶液检验溶液中含有的Fe2+ |
|
| D. | 用溶解、过滤的方法分离CaCl2和NaCl固体混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
①水分子的电子式为H+ 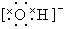 ②离子半径由小到大的顺序是:Mg2+<Na+<Cl-<S2-
②离子半径由小到大的顺序是:Mg2+<Na+<Cl-<S2-
③氮分子的电子式为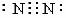 ④只含有离子键的化合物才是离子化合物
④只含有离子键的化合物才是离子化合物
A.①② B.③④ C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
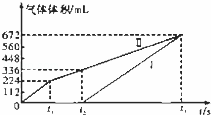
常温下用惰性电极电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(以下气体体积已换算成标准状况下的体积).根据图中信息回答下列问题.
(1)通过计算推测:
①原混合溶液中NaCl和CuSO4的物质的量浓度.
c(NaCl)= 0.1 mol•L﹣1,c(CuSO4)= 0.1 mol•L﹣1.
②t2时所得溶液的pH= 1 .
(2)若用惰性电极电解NaCl和CuSO4的混合溶液200mL,经过一段时间后两极均得到224mL气体,则原混合溶液中氯离子浓度的取值范围为 0<c(Cl﹣)<0.1mol/L ,铜离子浓度的取值范围为 c(Cu2+)=0.05mol/L .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com