
| A. | CH2CH2 | B. | CH2=C(CH3)2 | C. | CH3COH | D. | CH3C(CH2)2CH3 |
分析 A.乙烯的官能团为碳碳双键,其结构简式中应该标出碳碳双键;
B.CH2=C(CH3)2为2-甲基-1-丙烯,书写符合要求;
C.醛基的结构简式为-CHO,不能写成-COH;
D.C在有机物中的成键特点是满足4对共价键.
解答 解:A.乙烯的结构简式应该标出碳碳双键,乙烯的结构简式为:CH2=CH2,故A错误;
B.CH2=C(CH3)2为2-甲基-1-丙烯,该结构简式符合书写要求,故B正确;
C.乙醛的结构简式为CH3CHO,不能写出CH3COH,故C错误,
D.该化合物中第二个碳不满足4对共价键的要求,故D错误,故选B.
点评 本题考查常见有机物的结构简式判断,难度不大.注意掌握结构简式的概念及表示方法.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
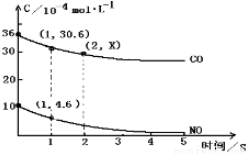
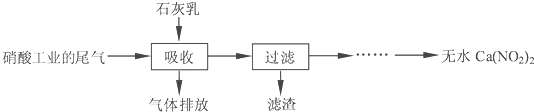
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的状态与反应热有关 | B. | 物质的状态与生成物有关 | ||
| C. | 可以具体说明反应进行的情况 | D. | 可以具体说明反应发生的条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
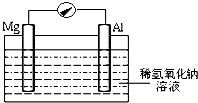 近年来,镁在汽车、航空、航天、机械制造、军事等产业中应用迅猛发展.
近年来,镁在汽车、航空、航天、机械制造、军事等产业中应用迅猛发展.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
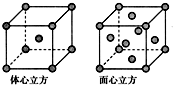 A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的p亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子.
A、B、C、D为前四周期元素.A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的p亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com