
| A. | 绿色化学的核心是利用化学原理从源头上减少和消除工农业生产对环境的污染 | |
| B. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成混合物具有丁达尔效应 |
分析 A.绿色化学的核心是从源头上减少或消除对环境的影响;
B.光导纤维的主要成分是二氧化硅以及二氧化硅能与氢氧化钠溶液反应,生成硅酸钠和水;
C.防氧化就是防止氧气的进入并与之反应,防受潮就是防止水分的进入;
D.胶体分散质粒子直径大小为1-100纳米,颗粒物直径大小2.5×10-6m>100纳米.
解答 解:A.绿色化学的核心是利用化学原理从源头上减少和消除工农业生产等对环境的污染,不是先造成环境污染,然后再处理,故A正确;
B.二氧化硅能用于制光导纤维、二氧化硅能与氢氧化钠溶液反应,生成硅酸钠和水,所以光导纤维遇强碱会“断路”,故B正确;
C.在食品袋中放入盛有硅胶和铁粉的透气小袋,硅胶(具有吸湿性)能吸收水分,铁是较活泼的金属,具有还原性,能防止食品被氧化,故C正确;
D.胶体分散质粒子直径大小为1-100纳米,颗粒物直径大小2.5×10-6m>100纳米,因此这些细颗粒物分散在空气中形成的混合物是浊液而不是胶体,因此不具有丁达尔效应,故D错误.
故选D.
点评 本题考查环境污染及治理、二氧化硅和干燥剂等,侧重于化学与人体健康的考查,为高考常见题型和高频考点,明确硅胶和铁粉防止食物受潮、氧化变质原理,掌握硅、二氧化硅的用途是解答的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )| A. | 合金的熔点通常比组分金属高,硬度比组分金属小 | |
| B. | 已知Ga处于ⅢA族,可推知氮化镓化学式为Ga3N2 | |
| C. | 用金属铝与V2O5冶炼钒,铝作还原剂 | |
| D. | 合金的化学性质一般与其各成分金属的化学性质不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔融的氯化钠是电解质 | |
| B. | 盐酸溶液属于非电解质 | |
| C. | 雾属于胶体,当用激光笔照射时,可以看到丁达尔现象 | |
| D. | 置换反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 上述实验证明了氧化性:Fe3+>Fe2+>Cu2+ | |
| B. | 上述实验证明了Fe2+既有氧化性又有还原性 | |
| C. | 实验①中的化学反应是置换反应 | |
| D. | 向三个实验后的溶液中加入足量NaOH溶液振荡,最终都有Fe(OH)3生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
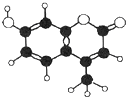 羟甲香豆素是一种激光染料,应用于可调谐染料激光器.羟甲香豆素分子模型如图所示,下列有关叙述错误的是( )
羟甲香豆素是一种激光染料,应用于可调谐染料激光器.羟甲香豆素分子模型如图所示,下列有关叙述错误的是( )| A. | 能使高锰酸钾溶液褪色 | |
| B. | 能与溴水发生取代反应和加成反应 | |
| C. | 分子式为C10H9O3 | |
| D. | 1mol羟甲香豆素最多能与3molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | b电极上发生氧化反应 | |
| B. | b电极附近溶液的pH增大 | |
| C. | a电极反应式:C6H10O5+24e-+7H2O═6CO2↑+24H+ | |
| D. | 中间室:Na+移向左室,Cl-移向右室 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,不可能具有的性质是( )
,不可能具有的性质是( )| A. | ① | B. | ①⑤⑥ | C. | ①③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 | |
| B. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| C. | 原电池中电流由正极流向负极,阳离子向正极移动 | |
| D. | 用惰性电极电解AgNO3溶液一段时间后,加入一定质量Ag粉,溶液能恢复原状 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| … | A | ||||||
| B | C | D |
| A. | 元素C在元素周期表d区 | |
| B. | D的电子排布式为1s22s22p63s23p5 | |
| C. | A氢化物沸点高于D的氢化物沸点 | |
| D. | A和B的离子中,半径较小的是B的离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com