
【题目】下列物质性质与用途的对应关系不正确的是
选项 | 性质 | 用途 |
A | 次氯酸有强氧化性 | 用作漂白剂 |
B | 氧化铝熔点很高 | 制造耐火坩埚 |
C | 硅有导电性 | 制造光导纤维 |
D | 硫酸有酸性 | 用于金属加工前的酸洗 |
A. A B. B C. C D. D
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
【题目】植物可以通过光合作用在体内合成有机物,被称为生物质(以淀粉为代表),具有广阔的应用前景。已知生物质的主要转化途径及主要产物如图所示:
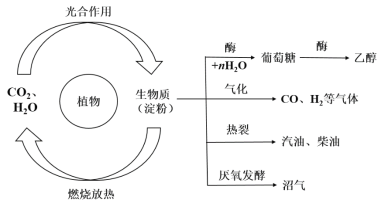
请回答:
(1)农村燃烧沼气供能的反应类型为下列的______。
A.吸热反应 B.放热反应 C.氧化还原反应 D.非氧化还原反应
(2)写出葡萄糖的化学式________________,上图由葡萄糖得到乙醇的反应中另一种气体产物的结构式为__________________。
(3)下列说法不正确的是______。
A.生物质中的能量本质上来自于太阳能
B.生物质气化产物中所含的能量既属于化学能,又属于生物质能
C.上图中生物质的所有转化均为化学反应
D.直接燃烧生物质是一种高效利用能源的方式
(4)已知18 g的葡萄糖固体被氧气完全氧化生成两种气体产物时放出热量254 kJ,写出该反应的热化学方程式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X和Y的原子序数都小于18,两者能组成化合物X2Y3,已知X的原子序数为n,则Y的原子序数不可能是( )
A.n+1B.n-5C.n+3D.n-6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应用化学反应原理知识解决下列问题
(1)写出醋酸(CH3COOH) 的电离方程式: _____________。
(2)明矾净水的原理为(用离子方程式表示)____________________________。
(3)一定条件下,56g金属铁与足量CO2气体完全反应生成碳单质和氧化铁固体时,放出117kJ热量,该反应的热化学方程式为_______________________。
(4) 现有浓度为0.1mol/L 的三种电解质溶液①NaHCO3 ②Na2CO3 ③NaOH 这三种溶液的pH 由小到大的顺序是__________________ (填编号)。
(5)常温下,下列事实能证明HA是弱电解质的是________ (填编号)。
a.某NaA溶液的pH=9
b.用HA 溶液做导电实验,灯泡很暗
c.等物质的量浓度、等体积的硫酸和HA溶液分别与足量锌反应,硫酸产生的氢气多d.0.1mol/LHA 溶液的pH≈2.8
(6)已知在100℃时,水的离子积为1×10-12,此时将 pH= 11 的 NaOH 溶液V1 L 与pH=2的H2SO4溶液V2 L均匀混合后,若所得混合溶液的pH=10,则V1: V2为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滑雪是冬奥会的主要项目之一。下列滑雪用品涉及到的材料属于合金的是
A. 滑雪板底板——塑料 B. 滑雪杖杆——铝材(铝、镁等)
C. 滑雪手套——合成橡胶 D. 滑雪服面料——尼龙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有下列几种物质:A.石墨和C60 B.35Cl和37Cl C.CH3CH=CHCH3和(CH3)2C=CH2 D.丁烷和新戊烷 E.![]() F.乙醇和二甲醚 G.间二甲苯和异丙苯
F.乙醇和二甲醚 G.间二甲苯和异丙苯
请把合适字母填入以下横线里:
①属于同分异构体的是____________ ②属于同系物的是_________③属于同种物质的是 ________。
(2)按要求填空
①画出羟基和乙烯的电子式:羟基 __________,乙烯 __________。
②用系统命名法给下列有机物命名
![]() ___________________________;
___________________________;
![]() ___________________________________;
___________________________________;
(3) 该有机物中含有的官能团的名称为____________.
该有机物中含有的官能团的名称为____________.
(4) 某些有机化合物的模型如图所示.

回答下列问题:
①属于比例模型的是___________(填“甲”、“乙”、“丙”、“丁”或“戊”,下同).
②存在同分异构体的是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2. 80 g部分被氧化成氧化镁的镁条完全溶于50. 0 mL硫酸溶液后,滴加2. 00 mol·Lˉ1氢氧化钠溶液,恰好完全沉淀时用去200. 0 mL。将所得的沉淀灼烧、冷却后称量得固体质量为4. 40 g。
请计算:
(1)质量为4. 40 g的固体是____________(填化学式)。
(2)镁条中氧化镁和镁的物质的量之比n(MgO)︰n(Mg)=____________。
(3)在与50. 0 mL硫酸溶液反应前被氧化的镁的质量是_____________g。
(4)上述硫酸的物质的量浓度c(H2SO4)=_____________mol·Lˉ1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有300mL MgCl2溶液,密度为1.18g/cm3,其中Mg2+的质量分数为5.1%。
(1)求该溶液中氯离子的物质的量。(结果保留1位小数)_______________
(2)向其中加入200mL 5mol/L NaOH溶液,充分反应后,求溶液中Mg2+的物质的量浓度_______________。(溶液混合过程中体积变化忽略不计)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com