
【题目】在蒸发皿中用酒精灯加热蒸干下列物质的溶液然后灼烧,可以得到该物质的固体的是( )
A. AlCl3 B. MgSO4 C. (NH4)2CO3 D. NaHCO3
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是( )
A. 表示硫的燃烧热的热化学方程式S(s)+![]() O2(g)=SO3(g);ΔH=-315 kJ·mol-1
O2(g)=SO3(g);ΔH=-315 kJ·mol-1
B. 表示中和热的热化学方程式NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);ΔH=-57.3 kJ·mol-1
C. 表示H2燃烧热的热化学方程式H2(g)+![]() O2(g)=H2O(g);ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g);ΔH=-241.8 kJ·mol-1
D. 表示CO燃烧热的热化学方程式2CO(g)+O2(g)=2CO2(g);ΔH=-566 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组用如图装置制取溴苯并证明苯和液溴发生的是取代反应。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
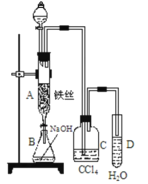
(1)写出 A 中发生反应的化学方程式_____________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是__________,写出有关反应的离子方程式____________。
(3)C中盛放 CCl4的作用是___________________。
(4)为证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液, 若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入___________,现象是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B为单质,C为化合物,能实现上述转化关系的是( )
![]()
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.①③
C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将9g由CO和H2组成的混合气体在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的质量为( )
A.8g B.9g C.12g D.13.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含2 mol NaOH、1 mol Ba(OH)2、2 mol NaAlO2的混合液中慢慢通入CO2至过量,下列有关说法正确的是( )
A.整个过程中共发生四个离子反应
B.根据现象可判断酸性强弱为:H2CO3>HAlO2>HCO![]()
C.通入3 mol CO2和通入5 mol CO2都只产生3 mol沉淀
D.整个过程中生成沉淀的物质的量与通入CO2的体积的图像如图所示

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合氯化铝晶体是介于 AlCl3和 Al(OH)3之间的一种水溶性无机高分子聚合物, 是一种高效无机水处理剂, 其制备原料主要是铝加工行业的废渣--铝灰,它主要含 Al2O3、 Al,还有一些不溶于酸的杂质.聚合氯化铝生产工艺流程如下:

(1)反应中副产品E是_________(用化学式表示);
(2)生产过程中可循环使用的物质是_________(用化学式表示);
(3)为使得到的晶体较纯净,生产过程中使pH升高的c 物质可选用_________(填编号);
a. NaOH b. Al c.氨水 d. A12O3 e. NaAlO2
(4)聚合氯化铝晶体的化学式可表示为: [A12(OH)nCl6-n·xH2O]m,实验室为测定化学式中n的值,进行如下实验:
①称取 ag晶体,制成粉末,加热至质量不再变化时,得到bg氧化铝固体.此过程可能用到的下列仪器有___________;(填编号)
a.蒸发皿 b.坩埚 c.研钵 d.试管
②另取ag晶体,进行如下操作:用A 酸溶解→加足量AgNO3溶液→操作c →烘干→称量为c g 固体.试剂A为_______,操作C为_________(填操作名称).n=_________(用含a、b、c的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁和铝的混合物投入100mL盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaoH溶液的体积关系如下图所示。 若不考虑金属和盐酸反应时HCI的挥发,则下列说法不正确的是( )
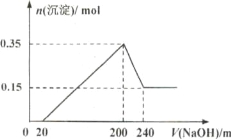
A.镁和铝的总质量为9 g
B.盐酸的物质的量浓度为10 mol/L
C.NaOH溶液的物质的量浓度为5 mol/L
D .生成的氢气在标准状况下的体积为11.2 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com