
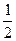 O2(g)="CO(g) " △H=
O2(g)="CO(g) " △H= 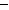 Q1kJ/mol ②2 CO(g)+ O2(g)=2CO2(g) △H=
Q1kJ/mol ②2 CO(g)+ O2(g)=2CO2(g) △H=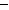 Q2kJ/mol (Q1、Q2均为正数)据此推断,下列说法正确的是
Q2kJ/mol (Q1、Q2均为正数)据此推断,下列说法正确的是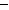 (Q1+Q2)kJ/mol
(Q1+Q2)kJ/mol科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
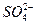 、
、 、
、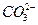 、CH3COO-离子的溶液中加入足量的硫酸,明显减少的阴离子有_________,明显增加的阴离子有_________,再加入足量BaCl2溶液,阴离子明显减少的是_________,增加的阴离子有_________,再加入足量AgNO3溶液,最后溶液中留下的的阴离子为_________。
、CH3COO-离子的溶液中加入足量的硫酸,明显减少的阴离子有_________,明显增加的阴离子有_________,再加入足量BaCl2溶液,阴离子明显减少的是_________,增加的阴离子有_________,再加入足量AgNO3溶液,最后溶液中留下的的阴离子为_________。查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.奥运火炬燃烧时的能量转化主要是化学能转变为热能 |
| B.丙烷燃烧的热化学方程式为:C3H8+5O2═3CO2+4H2O△H=-2221.5kJ?mol-1 |
| C.相同物质的量的正丁烷和丙烷分别完全燃烧,前者需要的氧气多,产生的热量也多 |
| D.异丁烷比正丁烷稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若A2和B2的总能量之和大于生成的2AB的总能量,则反应放热 |
| B.若A2和B2的总能量之和小于生成的2AB的总能量,则反应放热 |
| C.若该反应为放热反应,则Q1+Q2<Q3 |
| D.若该反应为吸热反应,则Q1+Q2<Q3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.反应的化学方程式为5Y?X |
| B.t1时,Y的浓度是X浓度的1.5倍 |
| C.t2时,正、逆反应速率相等 |
| D.t3时,逆反应速率大于正反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2Fe3++S2-====2Fe2++S↓ | B.Fe3++H2S====Fe2++S↓+2H+ |
| C.2Fe3++H2S====Fe2++S↓+2H+ | D.2FeCl3+S2-====2FeCl2+S↓+2Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.奥运火炬燃烧时的能量转化主要是化学能转变为热能 |
| B.丙烷燃烧的热化学方程式为:C3H8+5O2==3CO2+4H2O△H=-2221.5kJ·mol-1 |
| C.相同物质的量的正丁烷和丙烷分别完全燃烧,前者需要的氧气多,产生的热量也多 |
| D.异丁烷比正丁烷稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com