
 卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
分析 (1)根据基态原子核外电子排布式中最后填入电子名称确定区域名称,溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子;
(2)F的非金属性很强,HF分子间易形成氢键;
(3)元素的第一电离能越大,元素失电子能力越弱,得电子能力越强,元素的第一电离能越小,元素失电子能力越强,得电子能力越弱,则越容易形成阳离子;
(4)I3-离子的中心原子形成2个I-I;最外层8个电子,则孤电子对对数为3,空间构型为直线型;离子晶体的晶格能与离子半径成反比,与离子所带电荷成正比;
(5)根据价层电子对互斥理论来确定其杂化方式,价层电子对个数=σ键个数+孤电子对个数;等电子体是具有相同的价电子数和相同原子数的微粒;
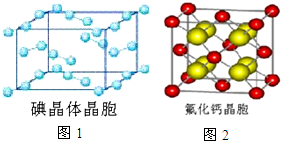
(6)碘为分子晶体,晶胞中占据顶点和面心,以此分析;
(7)利用均摊法确定该立方体中含有的离子,根据ρV=nM计算相对分子质量.
解答 解:(1)根据构造原理知,卤族元素最后填入的电子为p电子,所以卤族元素位于元素周期表的p区;溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,所以其价电子排布式为4s24p5,故答案为:p;4s24p5;
(2)HF分子之间存在氢键,使氢氟酸分子缔合,故答案为:氢键;
(3)卤族元素包含:F、Cl、Br、I、At元素,元素的第一电离能越小,元素失电子能力越强,得电子能力越弱,则越容易形成阳离子,根据表中数据知,卤族元素中第一电离能最小的是I元素,则碘元素易失电子生成简单阳离子,故答案为:I;
(4)I3-离子的中心原子形成2个I-I;最外层8个电子,则孤电子对对数为$\frac{1}{2}$×(7+1-2×1)=3,空间构型为直线型;离子晶体中离子电荷越多,半径越小离子键越强,离子晶体的晶格能越大,已知已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,所以发生的反应为CsICl2=CsCl+ICl,
故答案为:2;3;A;
(5)ClO2-中心氯原子的价层电子对数n=2+$\frac{7+1-2×2}{2}$=4,属于sp3杂化;等电子体具有相同的电子数目和原子数目的微粒,所以与ClO2-互为等电子体的分子为Cl2O、OF2等,故答案为:sp3;Cl2O或OF2;
(6)A.碘分子的排列有2种不同的取向,在顶点和面心不同,2种取向不同的碘分子以4配位数交替配位形成层结构,故A正确;
B.用均摊法可知平均每个晶胞中有4个碘分子,即有8个碘原子,故B错误
C.碘晶体为无限延伸的空间结构,构成微粒为分子,是分子晶体,故C错误;
D.碘晶体中的碘原子间存在I-I非极性键,且晶体中分子之间存在范德华力,故D正确;
故答案为:AD;
(7)该晶胞中含有钙离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,氟离子个数为8,棱上相邻的两个Ca2+的核间距为a cm,则晶胞体积V=a3,CaF2密度为=$\frac{m}{V}$=$\frac{M×4}{V{N}_{A}}$=ρ,则CaF2的相对分子质量M=$\frac{{a}^{3}ρ{N}_{A}}{4}$,故答案为:$\frac{{a}^{3}ρ{N}_{A}}{4}$.
点评 本题考查物质结构与性质,为高频考点,综合性强,涉及元素周期表、核外电子排布、分子结构与性质、电离能、晶体结构与性质、杂化轨道、等电子体、晶胞计算等,侧重对主干知识的考查,需要学生熟练掌握基础知识,题目难度中等.


科目:高中化学 来源: 题型:选择题
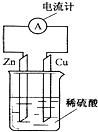
| A. | 锌片逐渐溶解 | B. | 电子由铜片通过导线流向锌片 | ||
| C. | 烧杯中溶液逐渐呈蓝色 | D. | 该装置能将电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H12O的醇,能在铜催化下被O2氧化为醛的同分异构体有5种 | |
| B. | 对苯二甲酸( )与乙二醇(HOCH2CH2OH)能通过加聚反应制取聚酯纤维( )与乙二醇(HOCH2CH2OH)能通过加聚反应制取聚酯纤维(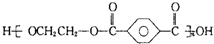 ) ) | |
| C. | 分子式为C9H10O2的有机物,①苯环上有两个取代基,②能与NaHCO3反应生成CO2气体,满足以上2个条件的该有机物的同分异构体有6种 | |
| D. | 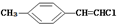 分子中的所有原子有可能共平面 分子中的所有原子有可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=CH2 | B. | CH2=CHCH=CH3 | C. | CH3CH=CHCH3 | D. | CH2=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeBr2溶液中通入少量Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 酸性高锰酸钾溶液中加入草酸:2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O | |
| C. | 硫代硫酸钠溶液中加入稀硫酸:2H++S2O32-═S↓+SO2↑+H2O | |
| D. | 将氧气通入酸性碘化钾溶液中:2I-+O2+4H+═I2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
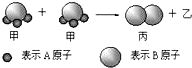
| A. | 根据阿伏加德罗定律可推知,1个乙分子中含有2个A原子 | |
| B. | Mr(甲)=Mr(乙)+Mr(丙) | |
| C. | 该反应一定属于氧化还原反应 | |
| D. | 该反应类型是分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可以作水果的催熟剂 | |
| B. | 石油分馏属于化学变化 | |
| C. | 苯燃烧时火焰明亮,伴有浓烟 | |
| D. | 冶炼金属是将金属从其化合物中还原出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HCl>HI | B. | O2和O3互为同素异形体 | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 干冰和冰为同一种物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com