
在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述不正确的是
A.白色沉淀是BaSO4和BaSO3
B.溶液的酸性增强
C.白色沉淀是BaSO4
D.FeCl3全部被还原为FeCl2
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是
A.CO2通入NaAlO2溶液中:AlO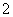 +CO2+H2O===Al(OH)3↓+CO
+CO2+H2O===Al(OH)3↓+CO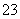
B.Al2O3与过量氨水:Al2O3+6NH3·H2O===2Al3++6NH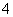
C.向AlCl3溶液中加入过量NaOH溶液:Al3++3OH-===Al(OH)3↓
D.向AlCl3溶液中滴入过量的氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH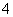
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.1 mol的镁、铝混合物溶于100 mL 2 mol·L-1H2SO4溶液中,然后再滴加1 mol·L-1NaOH溶液。请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。当V1=160 mL时,则金属粉末中n(Mg)=________ mol,V2=________ mL。
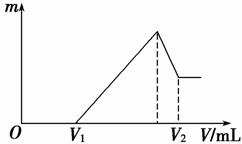
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=________ mL。
(3)若混合物仍为0.1 mol,其中镁粉的物质的量分数为a,用100 mL 2 mol·L-1的硫酸溶解此混合物后,再加入450 mL 1 mol·L-1的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各物质的转化关系如下图所示,其中A是一种高熔点固体,D是一种棕红色固体。
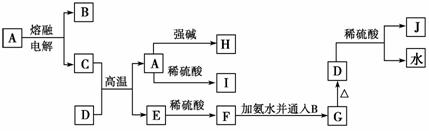
回答下列问题:
(1)C的化学式为________;J的化学式为________。
(2)写出由A生成H的离子反应方程式:_______________________________________。
(3)写出图中由F转化为G反应的离子方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生设计了如下方法对X盐进行鉴定:

由此分析,下列结论中正确的是
A.X中一定有Fe3+ B.Z中一定有Fe3+
C.Y为AgI沉淀 D.X一定为FeBr2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
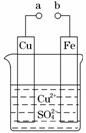 某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )
A.a 和 b 不连接时,铁片上会有金属铜析出
B.a 和 b 用导线连接时,铜片上发生的反应为:Cu2++2e-===Cu
C.无论 a 和 b 是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
D.a 和 b 分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
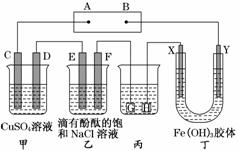
请回答:
(1)B极是电源的______________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明___________________,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为________。
(3)现用丙装置给铜件镀银,则H应是________________(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的pH是13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为测定镀锌铁皮锌镀层的厚度,将镀锌皮与足量盐酸反应,待产生的气泡明显减少时取出,洗涤,烘干,称重。关于该实验的操作对测定结果的影响判断正确的是
A.铁皮未及时取出,会导致测定结果偏小
B.铁皮未洗涤干净,会导致测定结果偏大
C.烘干时间过长,会导致测定结果偏小
D.若把盐酸换成硫酸,会导致测定结果偏大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com