
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
在一定温度下,反应A2(g) + B2(g) 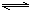 2AB(g)达到平衡的标志是
2AB(g)达到平衡的标志是
A、单位时间内生成nmolA2同时生成nmolAB
B、容器内的总物质的量不随时间变化
C、单位时间内生成2nmolAB的同时生成nmolB2
D、单位时间内生成nmolA2的同时生成nmolB2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语正确的是
A.乙醇的结构筒式:C2H6O
B.CH4的比例模型:
C.工业上制取粗硅的化学方程式: SiO2+C高温Si+CO2↑
D.电解饱和食盐水的离子方程式:2Cl-+2H2O===Cl2↑+2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钠(Na2FeO4)是一种饮用水的高效消毒剂,可由下列方法制得:
Fe2O3+3Na2O2高温2Na2FeO4+Na2O,关于该反应说法正确的是
A.Na2FeO4属于共价化合物
B.反应中Na2O2是氧化剂
C.生成l mol Na2FeO4,有6mol电子转移
D.在Na2FeO4中Fe为+4价,具有强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化铁在工业上具有广泛的应用。
I.据报道,一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应如下:
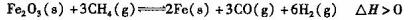
(1)若反应在2L的密闭容器中进行,5min后达到平衡,测得反应生成Fe的质量为l.12g。则该段时间内CH4的平均反应速率为 ________________ 。
(2)反应达到平衡后,保持其他条件不变,仅改变某一相关元素,下列说法正确的是 ________________(选填序号)。
a.若加入催化剂,v正增大,平衡向右移动
b.若温度升高,平衡常数K减小
c.若增大Fe2O3的量,平衡向右移动
d.若从反应体系中移走部分CO,可提高CH4的转化率
Ⅱ.工业上利用硫铁矿烧渣(主要成分为Fe2O3、A12O3、SiO2等)为原料提取Fe2O3,工艺 流程如下:试回答下列问题:
流程如下:试回答下列问题:
(3)结合下图,判断步骤ⅱ中调节溶液的pH范围_________________。
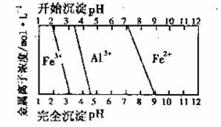
(4)写出步骤2中发生反应的离子方程式_____________________________,步骤2中分离出的滤渣的化学式是_________________。
(5)已知

 计算 的平衡常数为_____。
计算 的平衡常数为_____。
(6)在空气中煅烧FeCO3生成氧化铁的化学方程式为____________。
(7)结合所学化学知识,请你设计在实验室里从上述的硫铁矿烧渣中提取氧化铁的另一种简单方案_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于H2O2说法正确的是(NA代表阿伏加德罗常数) ( )
A.摩尔质量为34 g/mol B.每个H2O2分子含2NA个氧原子
C.2 mol H2O2含2 g氢元素 D.H2O2分子中H、O原子个数比为1:16
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述不正确的是
A.白色沉淀是BaSO4和BaSO3
B.溶液的酸性增强
C.白色沉淀是BaSO4
D.FeCl3全部被还原为FeCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com