
【题目】下列说法正确的是( )
A.H2(g)+I2(g) ![]() 2HI(g) ,其他条件不变,缩小反应容器体积,正逆反应速率不变
2HI(g) ,其他条件不变,缩小反应容器体积,正逆反应速率不变
B.C(s)+H2O(g) ![]() H2(g)+CO(g) ,碳的质量不再改变说明反应已达平衡
H2(g)+CO(g) ,碳的质量不再改变说明反应已达平衡
C.若压强不再随时间变化能说明反应 2A(?)+B(g) ![]() 2C(?) 已达平衡,则AC 不能同时是气体
2C(?) 已达平衡,则AC 不能同时是气体
D.C(s)+H2O(g) ![]() H2(g)+CO(g) ,将固态碳粉碎,不可加快化学反应速率。
H2(g)+CO(g) ,将固态碳粉碎,不可加快化学反应速率。
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)写出下列物质的分子式:含6个碳原子的链状单烯烃__________________________。
(2)在戊烷的各种同分异构体中,一氯代物种类最多的键线式是_________________。
(3)用系统命名法命名 :______________
:______________
(4)某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个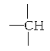 和一个-Cl。它的可能的结构有______________种
和一个-Cl。它的可能的结构有______________种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO、SO2是大气污染气体,利用化学反应是治理污染的重要方法。
Ⅰ.甲醇可以补充和部分替代石油燃料,缓解能源紧张,利用CO可以合成甲醇:CO+2H2![]() CH3OH(g)。一定条件下,在容积为VL的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。一定条件下,在容积为VL的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如图所示。
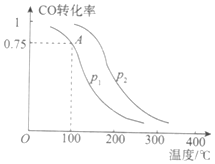
(1)下列能说明反应达到平衡状态的是_______(填序号)。
①v逆(CO)=2v正(H2)
②c(CO)=c(CH3OH)
③混合气体的平均相对分子质量不变
④单位时间内生成2n mol H2的同时生成n mol CH3OH
(2)该反应在A点的平衡常数K_________(用a和V表示)。
(3)写出既能增大v(CO)又能提高CO转化率的一项措施:________。
Ⅱ.某学习小组以SO2为原料,采用电化学方法制取硫酸。
(4)原电池原理:该小组设计的原理示意图(如图1所示),写出该电池正极的电极反应式_______。
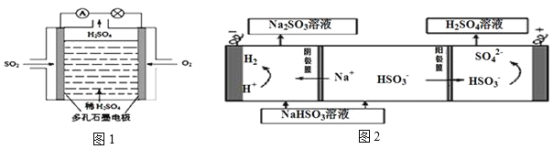
(5)电解原理:该小组用Na2SO3溶液充分吸收SO2得到NaHSO3溶液,然后电解该溶液制得了硫酸(原理如图2所示)。写出开始电解时阳极的电极反应式_______。
Ⅲ.硫代硫酸钠(Na2S2O3)俗称大苏打,有着广泛的用途。用SO2可制Na2S2O3。某小组同学制备、预测并探究硫代硫酸钠的性质(反应均在溶液中进行)。
预测 | 实验操作 | 实验现象 | |
探究1 | Na2S2O3溶液呈碱性 | 把pH试纸放在玻璃片上,用玻璃棒蘸取溶液滴在试纸上 | pH=8 |
探究2 | Na2S2O3具有还原性 | 向新制氯水中滴加Na2S2O3溶液 | 黄绿色颜色变浅,甚至褪去 |
(6)分析SO2能制备Na2S2O3的理论依据是_________。
(7)用离子方程式表示Na2S2O3溶液具有碱性的原因_________。
(8)探究2反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,3—二异丙烯基苯![]() 是重要的化工原料。下列有关1,3一二异丙烯基苯的说法正确的是
是重要的化工原料。下列有关1,3一二异丙烯基苯的说法正确的是
A.可以发生加成聚合反应B.不能使稀高锰酸钾溶液褪色
C.分子中所有原子共平面D.其苯环上的二氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50% B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式,回答下列各问:
① C(s)+1/2O2(g)=CO(g) ΔH =—110.4 kJ/mol
② C(s)+ O2(g)=CO2(g) ΔH =—393.5 kJ/mol
(1)C的燃烧热为______ kJ/mol 。
(2)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ 的热量。写出CH4燃烧热的热化学方程式__________________________________________________。
(3)工业上用CO2和H2反应合成甲醚。已知:
CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1
CH3OCH3(g)+H2O(g) = 2CH3OH(g) ΔH2=+23.4 kJ·mol-1
则2CO2(g)+6H2(g) = CH3OCH3(g)+3H2O(g) ΔH3=________kJ·mol-1。
(4)在恒温(500K)、体积为1.0L 的密闭容器中通入1.0 mol N2和1.0 mol H2发生合成氨反应N2 + 3H2![]() 2NH3,20 min 后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,该反应的热化学方程式为___________________________________。
2NH3,20 min 后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,该反应的热化学方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关含氯物质的说法不正确的是
A.向新制氯水中加入少量碳酸钙粉末能增强溶液的漂白能力
B.向NaClO溶液中通入少量的CO2的离子方程式:CO2+2ClO-+H2O=2HClO+CO32-(已知酸性:H2CO3>HClO>HCO3-)
C.向Na2CO3溶液中通入足量的Cl2的离子方程式:2Cl2+CO32-+H2O=CO2+2Cl-+2HClO
D.室温下,向NaOH溶液中通入Cl2至溶液呈中性时,相关粒子浓度满足:c(Na+)=2c(ClO-)+c(HClO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体育比赛中坚决反对运动员服用兴奋剂,倡导公平竞赛。某种兴奋剂的结构简式如图所示,下列有关该物质的说法中正确的是( )

A.遇FeCl3溶液显紫色,因为该物质属于苯酚的同系物
B.滴入KMnO4(H+)溶液,溶液的紫色褪去,能证明该物质分子中存在碳碳双键
C.该物质在一定条件下可以发生取代、加成、加聚、氧化、还原、消去等反应
D.1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4mol和7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,1LC2H5OH完全燃烧后生成的CO2分子个数约为![]()
B.20gD2O与20gH218O含有的中子数均为10NA
C.1mol·L-1Al(NO3)3溶液中含有3NA个NO3-
D.50mL12mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com