
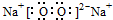 .
.
分析 (1)反应物中Na2CO3、CaCO3为离子晶体,SiO2为原子晶体;
(2)反应中涉及Na、C、Si、O、Ca五种元素,根据它们在周期中的位置分析;
(3)几种元素中金属性最强的短周期元素是Na,Na原子的核外电子排布为1s22s22p63s1;钠与氧气反应生成过氧化钠;
(4)破坏化学键要吸收能量;水分子为极性分子.
解答 解:(1)反应物中Na2CO3、CaCO3为离子晶体,离子晶体在熔融状态时能导电,SiO2为原子晶体,原子晶体在熔融状态下不导电;
故答案为:原子晶体;
(2)反应中涉及Na、C、Si、O、Ca五种元素,在周期表中相邻两元素为C、Si,其原子半径:Si大于C;处于同一周期元素为Na、Si,其名称是钠、硅;
故答案为:Si、C;钠、硅;
(3)几种元素中金属性最强的短周期元素是Na,Na原子的核外电子排布为1s22s22p63s1,所以钠原子核外有 4种不同能级的电子,钠与氧气反应生成过氧化钠,过氧化钠的电子式为: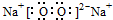 ;
;
故答案为:4;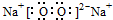 ;
;
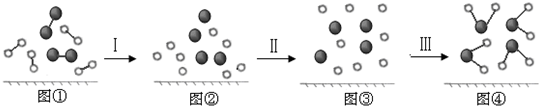
(4)过程Ⅰ中破坏化学键要吸收能量;图④中产生了由极性键构成的水分子,水分子空间结构为V形,结构不对称,电荷中心不重叠,为极性分子;
故答案为:吸热;极性.
点评 本题考查了晶体的类型、元素周期表的应用、电子式、化学键与能量、分子极性的判断等,把握原子的电子排布与元素的位置关系为解答的关键,注重基础知识的考查,题目难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
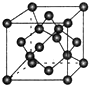 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1539 | 183 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 相关实验 | 预期目的 | |
| A | 向少量燃尽火柴头的浸泡液中滴加稀硫酸,AgNO3 | 验证火柴头含有氯元素 |
| B | 向两支装有等体积,等浓度的H2O2溶液试管中分别加入1mol等浓度的FeCl3溶液、CuSO4溶液 | 催化效果:Fe3+>Cu2+ |
| C | 向待测溶液中加NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝的气体 | 证明原溶液中含有NH4+ |
| D | 向等浓度的NaCl、KI混合液中逐滴加入AgNO3溶液先出现黄色沉淀 | K(sp),AgCl>AgI |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
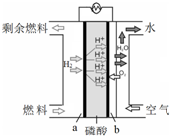
| A. | b极发生还原反应 | |
| B. | a极的反应式:H2+2OH--2e-═2H2O | |
| C. | 放电时,电子从b极经外电路流向a极 | |
| D. | 电池工作一段时间后,溶液中磷酸的浓度会升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用醋酸除去水垢:2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑ | |
| B. | 硫酸铁溶液中通入硫化氢气体:2Fe3++3H2S→2FeS↓+S↓+6H+ | |
| C. | 铝与氢氧化钠溶液反应:Al+2OH-→AlO2-+H2↑ | |
| D. | 已知25℃时,电离常数Ki (苯甲酸)>Ki1(H2CO3)>Ki (苯酚)>Ki2(H2CO3).常温下将水杨酸(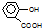 )与过量的Na2CO3溶液混合: )与过量的Na2CO3溶液混合: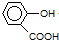 +2CO32-→ +2CO32-→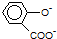 +2HCO3- +2HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com