
����Ŀ��H��һ���������ϵ���Ҫ�ɷ�֮һ����ϳ�·������(���ֲ���Ͳ��ַ�Ӧ������ȥ)��
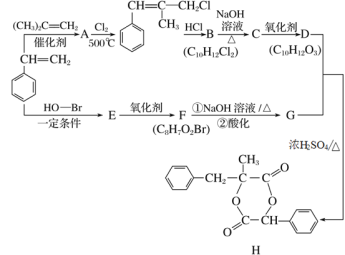
��֪����RCH=CH2+CH2==CHR��![]() CH2=CH2+RCH=CHR�䣻
CH2=CH2+RCH=CHR�䣻
��B�к˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ�ӡ�
��ش��������⣺
��1��(CH3)2C=CH2��ͬ���칹���д���˳���칹���л��������Ϊ________��
��2��A�ĺ˴Ź������׳������ϵ�H�⣬����ʾ________��壬�������Ϊ________��
��3��D�����к��еĺ���������������________��E�Ľṹ��ʽΪ__________________��
��4��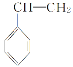 �����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ____________________________��D��G��Ӧ����H�Ļ�ѧ����ʽΪ_________________________________________��
�����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ____________________________��D��G��Ӧ����H�Ļ�ѧ����ʽΪ_________________________________________��
��5��G��ͬ���칹���У�ͬʱ����������������________��(�����������칹)��
�ٱ��Ķ�ȡ�������FeCl3��Һ������ɫ��Ӧ���ۺ�����COO�����ṹ
��6�����������ϳ�·�ߣ��Ա�ϩΪԭ��(���Լ���ѡ)������Ʊ�2��3���������ĺϳ�·��_______��
���𰸡� 2�D��ϩ 2 1��6 �ǻ����Ȼ� ![]()
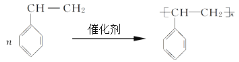
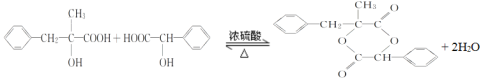 12 CH3CH==CH2
12 CH3CH==CH2![]() CH3CH==CHCH3
CH3CH==CHCH3![]()
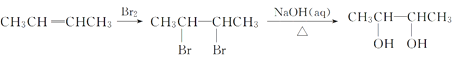
��������
��A�������ڼ��������·�Ӧ����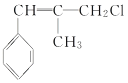 ����֪A�Ľṹ��ʽΪ
����֪A�Ľṹ��ʽΪ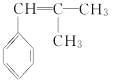 ���ʱ���ϩ��(CH3)2C===CH2������֪��Ϣϩ�����ֽⷴӦ����A��
���ʱ���ϩ��(CH3)2C===CH2������֪��Ϣϩ�����ֽⷴӦ����A��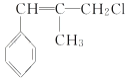 ��HCl��Ӧ����B�����B�ķ���ʽ��֪��Ӧ�Ƿ����ӳɷ�Ӧ��B�к˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ�ӣ���BΪ
��HCl��Ӧ����B�����B�ķ���ʽ��֪��Ӧ�Ƿ����ӳɷ�Ӧ��B�к˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ�ӣ���BΪ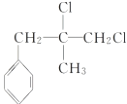 ��˳�ƿ�֪CΪ
��˳�ƿ�֪CΪ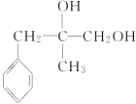 ��DΪ
��DΪ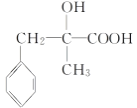 ������ϩ��HBrO�����ӳɷ�Ӧ����E��E������������C8H7O2Br��˵��E���ǻ����ӵ�Cԭ������2��Hԭ�ӣ���EΪ
������ϩ��HBrO�����ӳɷ�Ӧ����E��E������������C8H7O2Br��˵��E���ǻ����ӵ�Cԭ������2��Hԭ�ӣ���EΪ![]() ��C8H7O2BrΪ
��C8H7O2BrΪ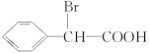 ��F������������Һ������ˮ�⡢�ữ�õ�G����GΪ
��F������������Һ������ˮ�⡢�ữ�õ�G����GΪ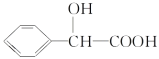 ��D��G����H��HΪ
��D��G����H��HΪ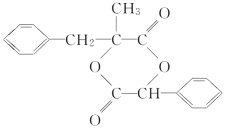 ��
��
(1)(CH3)2C===CH2��ͬ���칹����CH3CH===CHCH3����˳���칹������ϵͳ�����������л���Ļ�ѧ����Ϊ2��ϩ��(2) 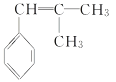 �������ϵ�H�⣬����2�ֵ�Ч�⣬�˴Ź���������ʾ2��壬�������Ϊ1��6��(3)
�������ϵ�H�⣬����2�ֵ�Ч�⣬�˴Ź���������ʾ2��壬�������Ϊ1��6��(3) 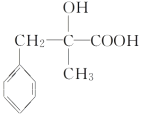 �����к��еĺ����������������ǻ����Ȼ���E�Ľṹ��ʽΪ
�����к��еĺ����������������ǻ����Ȼ���E�Ľṹ��ʽΪ![]() ��(4)
��(4) 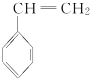 ���ӽṹ�к���̼̼˫�������Է����Ӿ۷�Ӧ����Ӧ�Ļ�ѧ����ʽΪ
���ӽṹ�к���̼̼˫�������Է����Ӿ۷�Ӧ����Ӧ�Ļ�ѧ����ʽΪ ��
��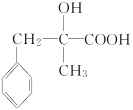 ��
��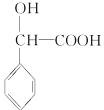 ����������Ӧ������H�Ļ�ѧ����ʽΪ
����������Ӧ������H�Ļ�ѧ����ʽΪ ��(5)
��(5) 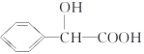 ��ͬ���칹���У�ͬʱ���������������ٵĶ�ȡ�������ȡ�������ڡ��估��λ������FeCl3��Һ������ʾ��Ӧ˵�����з��ǻ����ۺ�����COO�����ṹ���������Ȼ�Ҳ��������������������Ȼ���ֻ�С�CH2COOH����ʱ����3��������������������HCOOCH2����CH3COO������COOCH3����ʱ����9����������������Ĺ���12�������(6)�Ա�ϩΪԭ���Ʊ�2,3�������ĺϳ�·��ΪCH3CH==CH2CH3CH=CH2CH3CH==CHCH3
��ͬ���칹���У�ͬʱ���������������ٵĶ�ȡ�������ȡ�������ڡ��估��λ������FeCl3��Һ������ʾ��Ӧ˵�����з��ǻ����ۺ�����COO�����ṹ���������Ȼ�Ҳ��������������������Ȼ���ֻ�С�CH2COOH����ʱ����3��������������������HCOOCH2����CH3COO������COOCH3����ʱ����9����������������Ĺ���12�������(6)�Ա�ϩΪԭ���Ʊ�2,3�������ĺϳ�·��ΪCH3CH==CH2CH3CH=CH2CH3CH==CHCH3![]()
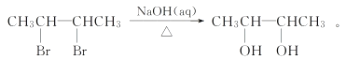



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��I�ֱ��ʾ��ѧ��ѧ�г�����һ�����ʣ�����֮�����ϵ����ͼ��ʾ(���ַ�Ӧ�������û���г�)����֪HΪ��̬�����A��I���ǽ������ʣ�F�Ǻ��ɫ������ˮ�ij�������A��B��C��D��E��F���������о���ͬһ��Ԫ�ء�
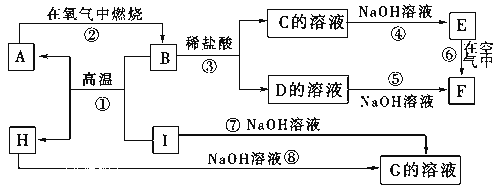
����д���пհף�
��1��A��B��C��D��E��F����������������ͬһ��Ԫ�ص�������________��
��2����Ӧ�۵����ӷ���ʽΪ________________________
��Ӧ��Ļ�ѧ����ʽΪ_____________________________________
��3����Ӧ�����е�������______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ٵ�����������������ڴ��� �еĹ����ǻ�����������Ҫ����֮һ��
(1).��֪:N2(g)+O2(g)=2NO (g) ��H=+180.5kJ/mol
C(s )+ O2(g)=CO2(g) ��H =-393.5kJ/mo1
2C(s)+ O2(g) =2CO(g) ��H=-221kJ/mol
��ij��Ӧƽ�ⳣ������ʽΪ: k=[c(N2)��c2(CO2)]/[c2(NO)��c2(CO)]����д���˷�Ӧ���Ȼ�ѧ��ʽ________________________��
(2)N2O4��һ�������¿ɷ����ֽ�: 2 N2O5(g)![]() 4NO2(g) +O2 (g)��ij�¶��²�ú����ܱ�������N2O4Ũ����ʱ��ı仯���±���
4NO2(g) +O2 (g)��ij�¶��²�ú����ܱ�������N2O4Ũ����ʱ��ı仯���±���
t /min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
c(N0)/(mol/L) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
�ٷ�Ӧ��ʼʱ��ϵѹǿΪP0��3.00minʱ��ϵѹǿΪP1����P1:P0 =__________2.00min~5.00min �ڣ�O2��ƽ����Ӧ����Ϊ________________��
��һ���¶��£��ں����ܱ���������һ����N2O5���и÷�Ӧ�����жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����________��
a.������ѹǿ���ٱ仯 b.NO2��O2 ������ȱ��ֲ���
c.2V��( NO2)=v��(N2O5) d.�����ƽ����Է�������Ϊ43.2.�ұ��ֲ���
(3)����̿��ԭNO2�ķ�ӦΪ: 2NO2(g)+2C (s)![]() N2(g)+2CO2(g)���ں��������£�1mo1NO2����������̿�����÷�Ӧ�����ƽ��ʱNO2��CO2��������Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ����A��B��C ������NO2��ת�������Լ��_____��(�A������B����C��)��
N2(g)+2CO2(g)���ں��������£�1mo1NO2����������̿�����÷�Ӧ�����ƽ��ʱNO2��CO2��������Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ����A��B��C ������NO2��ת�������Լ��_____��(�A������B����C��)��
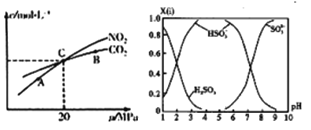
�ڼ���C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp=_________MPa (K��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
(4)ֱ���ŷź�SO2���������γ����꣬Σ������������NaOH���գ����ú������(H2SO3 ��HSO3-��SO32- )�����ڷ�Ӧ����ܱ��У����ǵ�����������X(i)����ҺpH�Ĺ�ϵ��ͼ��ʾ��
������0.lmol/LNaOH ��Ӧ�����Һ���ֵ���ҺΪpH=8ʱ����Һ�и�����Ũ���ɴ�С��˳����____________________��
(5)ʵ�鱷��NH4HSO3��Һ�У�![]() ������Һ��pHΪ_____�������Һ�мӰ�ˮʹ��Һ������ʱ��
������Һ��pHΪ_____�������Һ�мӰ�ˮʹ��Һ������ʱ��![]() =______________��(��֪: H2SO3��Ka1=1.5��10-2��Ka2=1.0��10-7)��
=______________��(��֪: H2SO3��Ka1=1.5��10-2��Ka2=1.0��10-7)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������úȼ�ջ����������Ⱦ��Ϊ���θ���Ⱦ��ij����������µ����۷�����ͬʱ�ɵõ�������Ʒ���ù���������ͼ��ʾ��������������ȷ����

A���ù����пɵõ�������ƷH2SO4
B���ù��������dz�ȥúȼ��ʱ������SO2
C���ù����л��ϼ۷����ı��Ԫ��ΪFe��S
D��ͼ���漰���ķ�Ӧ֮һΪFe2(SO4)3 + SO2 + 2H2O == 2FeSO4 + 2H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������н��з�Ӧ��X2(g)��Y2(g)![]() 2Z(g)����֪X2��Y2��Z����ʼŨ�ȷֱ�Ϊ0.1 mol��L��1��0.3 mol��L��1��0.2 mol��L��1����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п�����(����)
2Z(g)����֪X2��Y2��Z����ʼŨ�ȷֱ�Ϊ0.1 mol��L��1��0.3 mol��L��1��0.2 mol��L��1����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п�����(����)
A. ZΪ0.3 mol��L��1 B. Y2Ϊ0.4 mol��L��1
C. X2Ϊ0.2 mol��L��1 D. ZΪ0.4 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�־���ǿ�����ԡ���ʴ�Ե�ǿ�ᣬ�仹ԭ����������Ũ�ȵIJ�ͬ���б仯����������˵������Ũ��Խ�ߣ�ƽ��ÿ��������õ��ĵ�����Խ�٣�Ũ����Ļ�ԭ������ҪΪNO2��ϡ����Ļ�ԭ����ΪNO��ʵ�����У�����Cu��ŨHNO3��Ӧ��ȡNO2����Cu��ϡHNO3��Ӧ��ȡNO��
(1)��д��ʵ��������Cu��ϡHNO3��Ӧ��ȡNO�Ļ�ѧ����ʽ����˫���ű������ӵ�ת�Ʒ�����Ŀ_________________
(2)64gCu��������ŨHNO3��Ӧ��ͭȫ�����ú��ռ���22.4L����(��״����)����Ӧ�����ĵ�HNO3�����ʵ�����_________(����ĸ����)��
A.0.5mol B. 1.0mol C. 2.0mol D. 3.0mol
����������ֱ���_______________�������ʵ���֮����_______________
(3)ʵ����������ɱ���ԭΪNO2��NO��Ũ�ȸ�ϡʱ���ỹ���Ա���ԭΪN2O��N2��NH4NO3�ȣ��뽫����3�����ʣ�FeSO4��Fe(NO3)3��Fe2(SO4)3�ֱ����������Ӧ�ĺ����ϣ�����ƽ�÷�Ӧ�Ļ�ѧ����ʽ��___HNO3+_______�� _______+ _______ +___ NO��+___H2O
(4)����Ļ�ԭ����NO��NO2��N2O�ȶԻ������и����ã�Ϊ�˿ɳ�����չ��������������һ���¸���--����ɫ��ѧ������Ҫ��Ӿ��á������ͼ�������ƿ��еĻ�ѧ��Ӧ���������ɵ���ͭ��ȡ����ͭ�ķ��������ҷ��ϡ���ɫ��ѧ������_______(����ĸ����)��
A��Cu![]() Cu(NO3)2
Cu(NO3)2
B��Cu![]() CuO
CuO![]() Cu(NO3)2
Cu(NO3)2
C��Cu![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2![]() Cu(NO3)2
Cu(NO3)2
D��Cu![]() CuSO4
CuSO4![]() Cu(NO3)2
Cu(NO3)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��������£���һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2 L���ܱ������з�����Ӧ��N2O4(g)![]() 2NO2(g)����H>0����Ӧ�����и����ʵ����ʵ���Ũ��(c)��ʱ��(t)�ı仯������ͼ��ʾ��
2NO2(g)����H>0����Ӧ�����и����ʵ����ʵ���Ũ��(c)��ʱ��(t)�ı仯������ͼ��ʾ��
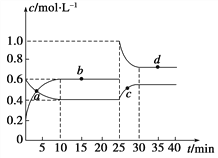
��1�����¶��£��÷�Ӧ��ƽ�ⳣ��Ϊ______________��
��2��a��b��c��d�ĸ����У���ʾ��ѧ��Ӧ����ƽ��״̬����________�㡣����㿪ʼ�״δﵽƽ��ʱ����NO2��ʾ�ķ�Ӧ����Ϊ____________��
��3��25 minʱ��������__________(��������ʵĻ�ѧʽ����������ʵ���)��ʹƽ�ⷢ�����ƶ���
��4��d���ӦNO2�����ʵ���Ũ��________(��������������С��������������)0.8 mol��L��1��������____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ�м���Na2O2�����ܴ����������������
A. NH4+��Ba2+��Cl![]() ��NO3- B. K+��AlO
��NO3- B. K+��AlO![]() ��Cl
��Cl![]() ��SO
��SO![]()
C. Ba2+��Mg2+��NO![]() ��HCO
��HCO![]() D. Na+��Cl
D. Na+��Cl![]() ��CO
��CO![]() ��SO
��SO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ƾ��壨Na2S2O3��5H2O��M=248 g��mol1����������Ӱ������ԭ�����ش��������⣺
��1����֪��Ksp(BaSO4)=1.1��1010��Ksp(BaS2O3)=4.1��105����������������г�������������ʣ�ѡ�������Լ����ʵ�鷽�����м��飺
�Լ���ϡ���ᡢϡH2SO4��BaCl2��Һ��Na2CO3��Һ��H2O2��Һ
ʵ�鲽�� | ���� |
��ȡ������Ʒ�������������ˮ | �ڹ�����ȫ�ܽ����ɫ������Һ |
��___________ | ��___________���д̼���������� |
�ݾ��ã�___________ | ��___________ |
��2������K2Cr2O7����Һ�����ⶨ��������ƵĴ��ȡ��ⶨ�������£�
����Һ���ƣ���ȡ1.2000 gij��������ƾ�����Ʒ��������в���ȴ������ˮ��__________���ܽ⣬��ȫ�ܽ��ȫ��ת����100 mL��_________�У�������ˮ��____________��
�ڵζ���ȡ0.00950 mol��L1��K2Cr2O7����Һ20.00 mL�������ữ��������KI��������Ӧ�� Cr2O72+6I+14H+![]() 3I2+2Cr3++7H2O��Ȼ���������������Ʒ��Һ�ζ���������ɫ��������Ӧ��I2+2S2O32
3I2+2Cr3++7H2O��Ȼ���������������Ʒ��Һ�ζ���������ɫ��������Ӧ��I2+2S2O32![]() S4O62+2I�����������Һ��Ϊָʾ���������ζ�������Һ__________����Ϊ�յ㡣ƽ�еζ�3�Σ���Ʒ��Һ��ƽ������Ϊ24.80 mL������Ʒ����Ϊ_________%������1λС������
S4O62+2I�����������Һ��Ϊָʾ���������ζ�������Һ__________����Ϊ�յ㡣ƽ�еζ�3�Σ���Ʒ��Һ��ƽ������Ϊ24.80 mL������Ʒ����Ϊ_________%������1λС������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com