
 已知:A、D、E、G、J、L、M七种元素的原子序数依次增大.A在所有元素中原子半径最小;D原子核外电子有6种不同运动状态;G与E、J均相邻;A、G、J三种元素的原子序数之和为25;J2-和L+有相同的核外电子排布;M的质子数是25.请回答下列问题:
已知:A、D、E、G、J、L、M七种元素的原子序数依次增大.A在所有元素中原子半径最小;D原子核外电子有6种不同运动状态;G与E、J均相邻;A、G、J三种元素的原子序数之和为25;J2-和L+有相同的核外电子排布;M的质子数是25.请回答下列问题: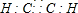 、
、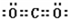 .
.分析 A、D、E、G、J、L、M七种元素.它们的原子序数依次增大,A在所有元素中原子半径最小,则A是H元素;
D原子核外电子有6种不同运动状态,则D为C元素;
G与E、J均相邻,A、G、J三种元素的原子序数之和为25,A的原子序数是1,所以G和J的原子序数之和为24,其平均原子序数为12,所以G原子序数小于12、J原子序数大于12,J能形成负二价阴离子,所以J为S元素,则G原子序数为8,为O元素;
E原子序数大于D而小于G,所以E是N元素;
J2-和L+有相同的核外电子排布,则L是K元素;
M的质子数是25,则M为Mn元素,由此分析解答.
解答 解:(1)则M为Mn元素,其外围电子为其最外层电子,根据构造原理知元素Mn的基态原子外围电子排布式为3d54s2;甲烷、氨气和水,水的沸点最高,故答案为:3d54s2;H2O;
(2)G为氧元素,由氧元素组成的单质有氧气和臭氧,与臭氧分子互为等电子体且属于上述元素的阴离子有NO2-,故答案为:NO2-;
(3)乙炔和二氧化碳都是直线型非极性分子,其电子式为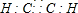 、
、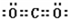 ,故答案为:
,故答案为: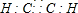 、
、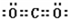 ;
;
(4)R是由4个E元素组成的一种不稳定的多原子单质分子,R分子中E原子杂化方式为sp3,则该分子为正四面体结构,其结构和白磷分子相似,故答案为:正四面体;
(5)将A2G2的溶液滴加到M的一种常见氧化物上,会产生G的一种单质,是过氧化氢在二氧化锰做催化剂的作用下分解产生氧气,方程式为:2H2O$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,故答案为:2H2O$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
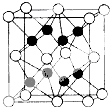
(6)电负性最大的元素是O元素,第一电离能最小的元素是K元素,二者生成化合物K2O,离子晶体中晶格能与电荷成正比、与离子半径成正比,钙离子电荷数大于钾离子、半径小于钾离子,所以晶格能较小的是K2O;该晶胞中白色球个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,黑色球个数=8,所以黑色和白色球个数之比为2:1,其化学式为K2O,所以白色球表示氧离子、黑色球表示钾离子,晶胞的边长为a×10-10cm,晶胞体积=(a×10-10cm)3,密度ρ=$\frac{m}{V}$=$\frac{\frac{M}{{N}_{A}}×4}{V}$=$\frac{\frac{94×4}{{N}_{A}}}{(a×1{0}^{-10})3}$g•cm-3=$\frac{\frac{94×4}{{N}_{A}}}{{a}^{3}}$g•cm-3=$\frac{4×94}{NA•a3}$g•cm-3,故答案为:K2O; $\frac{4×94}{NA•a3}$.
点评 本题考查物质结构和性质,涉及晶胞计算、晶格能、原电池原理等电子体等知识点,同时考查学生分析问题、解决问题能力,利用基本概念、基本理论解答即可,注意(4)中分子结构特点,知道4个N原子位置关系,为易错点.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 双氧水被称为绿色氧化剂,是因为其还原产物通常为O2,对环境没有污染 | |
| B. | 王水是浓硫酸和浓硝酸按体积比3:1配成的混合物,可以溶解Au、Pt | |
| C. | 氨水显弱碱性,浓度越大密度越大 | |
| D. | 新制备的氯水中存在三种分子,四种离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
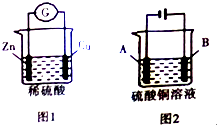
| A. | 图1装置将化学能转化为电能,电子由锌极经过稀硫酸进入铜极 | |
| B. | 利用图2装置可进行粗铜的精炼,则粗铜做A极 | |
| C. | 若A、B两电极均为铜,利用图2装置电解硫酸铜溶液,则电解后溶液的pH不变 | |
| D. | 利用图2装置可在铁上镀铜,则铁作B极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极有 O2 逸出 | |
| B. | 铜片上有 H2 逸出 | |
| C. | 电子通过导线由铜片流向锌片 | |
| D. | 正极附近的 SO42- 离子浓度逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
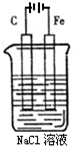 (1)如图是电解NaCl溶液的示意图.请回答下列问题:
(1)如图是电解NaCl溶液的示意图.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
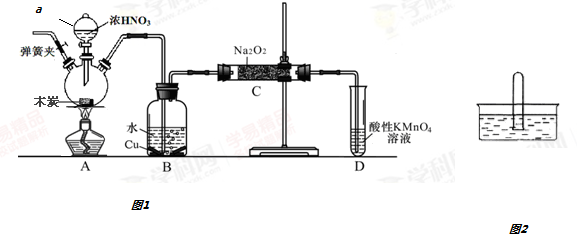
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
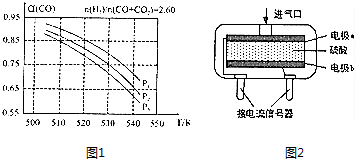 利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醛,主要反应如下:
利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醛,主要反应如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com