
| Vρ |
| M |
| M |
| NA△ |
| M |
| NA |
| V |
| NA |
| A、4个 | B、3 个 |
| C、2个 | D、1个 |
| m |
| M |
| m |
| V |
| Vρ |
| m |
| M |
| V |
| M |
| NA |


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
A、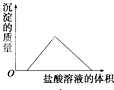 |
B、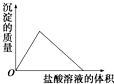 |
C、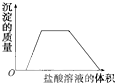 |
D、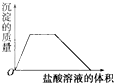 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 药品名称 | 熔点/℃ | 沸点(℃) | 密度 g/cm3 | 溶解性 |
| 正丁醇 | -89.5 | 117.7 | 0.8098 | 微溶于水、溶于浓硫酸 |
| 1-溴丁烷 | -112.4 | 101.6 | 1.2760 | 不溶于水和浓硫酸 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 试验次数 | 起 始 温 度T1/℃ | 终止温度T2/℃ | 平均温度差 (T2-T1)/℃ | ||
| H2SO4 溶液 | NaOH溶液 | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
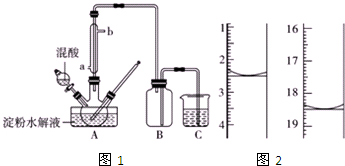 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热,搅拌和仪器固定装置均已略去)
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热,搅拌和仪器固定装置均已略去)查看答案和解析>>
科目:高中化学 来源: 题型:
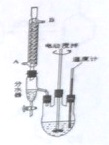 邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下:
邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com