
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
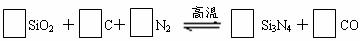
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应的氧化剂是 ,其还原产物是 ;
(3)该反应的平衡常数表达式为K=  ;
;
(4)若知上述反应为放热反应,则其反应热△H 零(填“大于”、“小于”或“等于”);升高温度,其平衡常数值 (填“增大”、“减小”或“不变”);
(5)若使压强增大,则上述平衡向 反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v(CO)=18mol/(L·min),则N2消耗速速率为v(N2)= mol/(L·min)。
【答案】
(1)3,6,2,1,6
(2)N2,Si3N4
(3)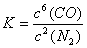 (或K=
(或K=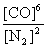 )
)
(4)小于;减小
(5)逆
(6)6
【解析】本题是一道主要考查化学反应速率和化学平衡的综合题。
(1)用化合价升降法配平
3SiO2+6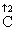 +2
+2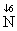 2
2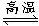 Si3N4+6CO
Si3N4+6CO
N2为氧化剂,C为还原剂,Si3N4为还原产物。
(2)因为N2、CO为气体,K=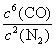 ;
;
反应热用ΔH来表示,ΔH<0,升高温度,平衡向吸热方向移动,即向逆反应方向移动,K减小,增大压强,平衡向气体体积减小的方向移动,即向逆反应方向移动。速率之比等于化学计量数之比,则N2消耗速率为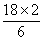 mol·(L·min)-1=6 mol·(L·min)-1。
mol·(L·min)-1=6 mol·(L·min)-1。


科目:高中化学 来源: 题型:
室温下,在0.2 mol·L-1 Al2(SO4)3溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是( )
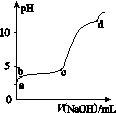
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为Al3++3OH- Al(OH)3
Al(OH)3
B.a~b段,溶液pH增大,Al3+浓度不变
C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀
D.d点时,Al(OH)3沉淀开始溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
[实验]制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
(1)下列有关制备银镜过程的说法正确的是 。
a.边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水。至最初的沉淀恰好溶解为止
b.将几滴银氨溶液滴入2 mL乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配制过程中,溶液的pH增大
[提出假设]
假设1:Fe1+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3能氧化Ag。
[设计实验方案,验证假设]
(2)甲同学从上述实验的生成物中检验出Fe3+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式: 。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示: NO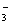 在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① ② …… | 若银镜消失,假设2成立。 若银镜不消失,假设2不成立。 |
[思考与交流]
(4)甲同学验证了假设1成立,若乙同学验证了假设2也成立。则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO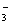 都氧化了Ag。
都氧化了Ag。
你是否同意丙同学的结论,并简述理由: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C 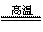 2AlN+3CO合成。下列叙述正确的是( )
2AlN+3CO合成。下列叙述正确的是( )
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41 g
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
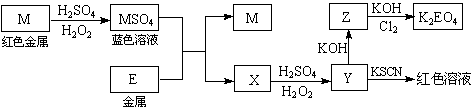
⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
⑵某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 、 。
⑶写出Cl2将Z氧化为K2EO4的化学方程式: 。
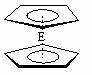
⑷由E制备的E(C2H5)2的结构如下图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为: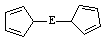 。核磁
。核磁 共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:
①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液
由于浓度不同而发生不同氧化还原反应的是
A.①③ B.③④ C.①② D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
衣康酸M是制备高效除臭剂,粘合剂等多种精细化学品的重要原料,可经下列反应路线得到(部 分反应条件略)。
分反应条件略)。
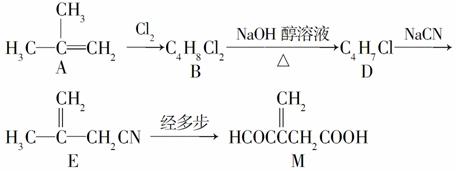
(1)A发生加聚反应的官能团名称是________,所得聚合物分子的结构型式是________(填“线型”或“体型”)。
(2)B→D的化学方程式为_________________________________。
(3)M的同分异构体Q是饱和二元羧酸,则Q的结构简式为________(只写一种)。
(4)已知:—CH2CN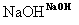 —CH2COONa+NH3,E经五步转变成M的合成反应流程为:
—CH2COONa+NH3,E经五步转变成M的合成反应流程为:
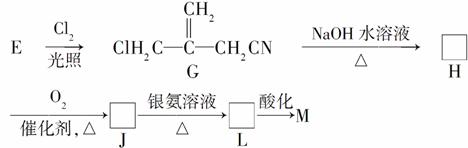
①E→G的化学反应类型为________,G→H的化学方程式为____________________。
②J→L的离子方程式为________________________________。
③已知:-C(OH)3-COOH+H2O,E经三步转变成M的合成反应流程为________________________________________
___________________________________________________________
(示例如上图;第二步反应试剂及条件限用NaOH水溶液、加热)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com