
根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
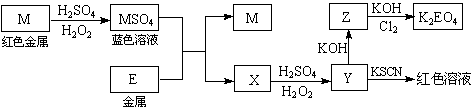
⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
⑵某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 、 。
⑶写出Cl2将Z氧化为K2EO4的化学方程式: 。
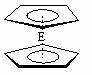
⑷由E制备的E(C2H5)2的结构如下图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为: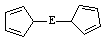 。核磁
。核磁 共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
【答案】
⑴Cu + H2O2 + H2SO4 = CuSO4 + 2H2O
⑵4Fe2++O2+4H+ 4Fe3++2H2O 2Fe3++2I-
4Fe3++2H2O 2Fe3++2I- 2Fe2++I2
2Fe2++I2
⑶10KOH + 3Cl2 + 2Fe(OH)3 = 2K2FeO4 + 6KCl + 8H2O
⑷1 3
【解析】M为红色金属,与酸反应生成蓝色溶液,推知M为Cu。
由Y中加KSCN得红色溶液,确定Y中 含有Fe3+,从而确定E为Fe。M为Cu,X为FeSO4,Y为Fe2(SO4)3,Z为Fe(OH)3,K2EO4为K2FeO4。
含有Fe3+,从而确定E为Fe。M为Cu,X为FeSO4,Y为Fe2(SO4)3,Z为Fe(OH)3,K2EO4为K2FeO4。
(2)FeSO4溶 液酸化后加入KI淀粉溶液变蓝色,说明有I2生成。其变化过程中相关离子方程式为4Fe2++O2+4H+
液酸化后加入KI淀粉溶液变蓝色,说明有I2生成。其变化过程中相关离子方程式为4Fe2++O2+4H+ 4Fe3++2H2O,2Fe3++2I-
4Fe3++2H2O,2Fe3++2I- 2Fe2++I2。
2Fe2++I2。
(4)根据题干信息,正确的结构中的氢原子化学环境完全相同,故在核磁共振氢谱中有1种峰;而错误的结构中氢原子有3种不同的化学环境,故有3种峰。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
室温下,用0.100 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 mol·L-1的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是( )
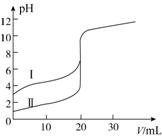
A.Ⅱ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20 mL
C.V(NaOH)=20.00 mL时,两份溶液中c(Cl-)=c(CH3COO-)
D.V(NaOH)=10.00 mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计及其对应的离子方程式均正确的是
A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ = Cu2+ + 2Fe2+
B.Na2O2与H2O反应制备O2 :Na2O2 + H2O = 2Na+ + 2OH- + O2↑
C.将氯气溶于水制备次氯酸:Cl2 + H2O = 2H+ + Cl- + ClO-
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO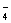 + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。
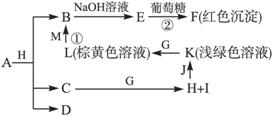
请回答下列问题:
(1)写出A的化学式_____________,C的电子式____________。
(2)比较Y与Z的原子半径大小___________ _>__________
_>__________ __(填写元素符号)。
__(填写元素符号)。
(3)写出反应②的化学方程式(有机物用结构简式表示)____________,举出该反应的一个应用实例________________________。
(4)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的化学方程式:____________________________________。
(5)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称____________、____________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)配平氧化还原反应方程式:

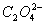 +
+
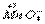 +
+ H+
H+ CO2↑+
CO2↑+ Mn2++
Mn2++ H2O
H2O
(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。
①第一份溶液中加入2滴酚酞试液,滴加0.25 mol·L-1 NaOH溶液至20 mL时,溶液由无色变为浅红色。该溶液被中和的H+的物质的量为___________________mol。
②第二份溶液中滴加0.10 mol·L-1酸性KMnO4溶液至16 mL时反应完全,此时溶液颜色由_____________变为___________。该溶液中还原剂的物质的量为________mol。
③原试样中H2C2O4·2H2O的质量分数为__________,KHC2O4的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
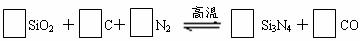
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应的氧化剂是 ,其还原产物是 ;
(3)该反应的平衡常数表达式为K=  ;
;
(4)若知上述反应为放热反应,则其反应热△H 零(填“大于”、“小于”或“等于”);升高温度,其平衡常数值 (填“增大”、“减小”或“不变”);
(5)若使压强增大,则上述平衡向 反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v(CO)=18mol/(L·min),则N2消耗速速率为v(N2)= mol/(L·min)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:
H2O2→H2O IO3-→I2 MnO4-→Mn2+ HNO2→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
A H2O2 B IO3-
C MnO4- D HNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物H是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下:
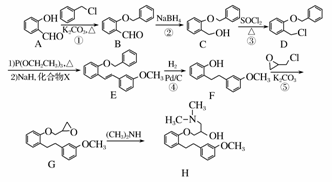
(1)化合物A中的含氧官能团为________和________。(填官能团名称)
(2)反应①→⑤中,属于取代反应的是________(填序号)。
(3)写出同时满足下列条件的B的一种同分异构体的结构简式:________________________________________________________________________。
Ⅰ.分子中含有两个苯环;
Ⅱ.分子中有7种不同化学环境的氢;
Ⅲ.不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
(4)实现D→E的转化中,加入的化合物X能发生银镜反应,X的结构简式为________。
(5)已知: 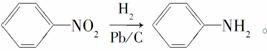 化合物
化合物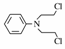 是合成抗癌药物美法伦的中间体,请写出以
是合成抗癌药物美法伦的中间体,请写出以 和
和 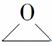 为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
H2C===CH2CH3CH2Br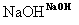 CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
某天然有机化合物A仅含C、H、O元素,与A相关的反应框图如下:
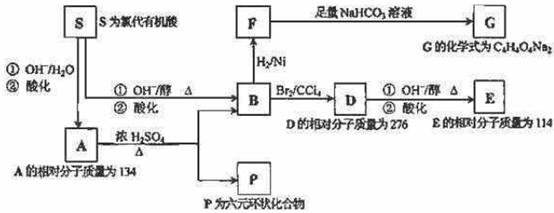
(1)写出下列反应的反应类型:
S→A第①步反应____________、B→D___________、D→E第①步反应__________、A→P____________。
(2)B所含官能团的名称是_______________________________。
(3)写出A、P、E、S的结构简式:
A:________________________、P:____________________、
E:________________________、S:____________________。
(4)写出在浓H2SO4存在并加热的条件下,F与足量乙醇反应的化学方程式:_________。
(5)写出与D具有相同官能团的D的所有同分异构体的结构简式:__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com