
【题目】下列关于溶液中离子的说法不正确的是( )
A.0.1mol?L﹣1的Na2CO3溶液中粒子浓度关系:c(Na+)═2c(CO ![]() )+2c(HCO
)+2c(HCO ![]() )+2c(H2CO3)
)+2c(H2CO3)
B.常温下,氢氧化钠溶液中滴入醋酸使溶液的pH=7,则混合溶液中醋酸已过量
C.0.2mol?L﹣1的HCl和0.1 mol?L﹣1的NH3?H2O等体积混合后溶液中的离子浓度关系:c(Cl﹣)>c (NH ![]() )>c(H+)>c (OH﹣)
)>c(H+)>c (OH﹣)
D.0.1mol?L﹣1的NaHS溶液中离子浓度关系:c(S2﹣)+c(OH﹣)═c(H+)+c(H2S)
【答案】C
【解析】解:A、0.1molL﹣1的Na2CO3溶液中物料守恒式为c(Na+)=2c(CO ![]() )+2c(HCO
)+2c(HCO ![]() )+2c(H2CO3),故A正确, B、醋酸和氢氧化钠恰好反应生成醋酸钠溶液呈碱性,若溶液呈中性需要醋酸过量,才可以使溶液显示中性,故B正确;
)+2c(H2CO3),故A正确, B、醋酸和氢氧化钠恰好反应生成醋酸钠溶液呈碱性,若溶液呈中性需要醋酸过量,才可以使溶液显示中性,故B正确;
C、0.2molL﹣1的HCl和0.1 molL﹣1的NH3H2O等体积混合后溶液中是HCl和NH4Cl的混合溶液,溶液中铵根离子水解,氢离子浓度大于铵根离子浓度,c(Cl﹣)>c(H+)>c (NH ![]() )>c (OH﹣),故C错误;
)>c (OH﹣),故C错误;
D、0.1molL﹣1的NaHS溶液中电荷守恒,c(Na+)+c(H+)=c(OH﹣)+c(HS﹣)+2c(S2﹣),物料守恒c(Na+)=c(HS﹣)+c(S2﹣)+c(H2S),带入计算得到c(S2﹣)+c(OH﹣)═c(H+)+c(H2S),故D正确;
故选C.


科目:高中化学 来源: 题型:
【题目】无色水溶液中能大量共存的一组离子是( )
A. NH4+、Ba2+、Br﹣、CO32﹣ B. Cl﹣、SO42﹣、Mg2+、H+
C. K+、Na+、SO42﹣、MnO4﹣ D. Na+、H+、NO3﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的溶液时,由于操作不慎,使液面略超过了容量瓶的刻度(标线),这时应采取的措施是
A.倾出标线以上的液体 B.吸出标线以上的溶液
C. 影响不大,不再处理 D.重新配制.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
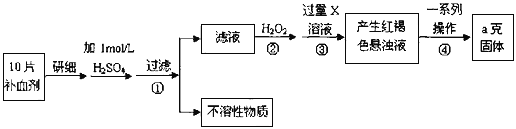
请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有__________________(填离子符号),检验滤液中还存在Fe2+的方法为_________________________________________。(注明试剂、现象)
(2)步骤②加入过量H2O2的目的:____________________________________________。
(3)步骤③中反应的离子方程式:_____________________________________________。
(4)若实验无损耗,则每片补血剂含铁元素的质量__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年以来,我国多地频现种种极端天气,二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素.
(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
①请结合上表数据,写出NO与活性炭反应的化学方程式 .
②上述反应的平衡常数表达式K= , 根据上述信息判断,T1和T2的关系是 .
A.T1>T2 B.T1<T2 C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是 .
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2 , 具体流程如图1所示:
①用离子方程式表示反应器中发生的反应: .
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是 .
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示.
通过a气体的电极是原电池的极(填“正”或“负”),b电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】治疗缺铁性贫血的常见方法是服用补铁药物,常采用更易被吸收的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水,但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中二价铁元素,设计并实施了如下实验:
![]()
试回答下列问题:
(1)试剂1是______________,试剂2是__________________。
(2)该同学预测加入试剂2后,溶液应依然为浅绿色,但这与实际现象不符,请用离子方程式解释实际现象的合理性:_________________,_______________。
(3)用离子反应方程式解释加入新制氯水后溶液变血红色的原因:______________________________________________。
(4)补铁药物的说明书中通常会有“与VC同服可增加本品吸收”的内容,向淡红色溶液中加入VC,片刻后溶液红色褪去,试从氧化还原角度解释补铁药物与VC同服的优点:___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,现有A、B、C、D、E、F六种常见化合物,已知它们的阳离子有K+、Ag+、Ca2+、Ba2+、Fe2+、Al3+ , 阴离子有Cl﹣、OH﹣、CH3COO﹣、NO3﹣、SO42﹣、CO32﹣ , 现将它们分别配成0.1mol/L的溶液,进行如下实验:(已知:室温下,饱和氢氧化钙溶液浓度约为0.00165 g/mL)
①测得溶液A、C、E呈碱性,且碱性为A>E>C;
②向B溶液中滴加Na2S溶液,出现难溶于强酸且阴阳离子个数比为1:2的黑色沉淀;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色.
根据上述实验现象,回答下列问题:
(1)写出下列化合物的化学式:A、B、C .
(2)实验④中白色沉淀变为红褐色对应的化学方程式:
(3)D与E的溶液反应离子方程式是: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com