
����Ŀ������Ӧ�úʹ������Ļ��������������������Ҫ���塣
��1������[CO(NH2)2]��һ�ָ�Ч���ʣ�Ҳ��һ�ֻ���ԭ�ϡ�
��������Ϊԭ����һ�������·�����Ӧ��
CO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g)��H=+133.6 kJ/mol�����ڸ÷�Ӧ������˵����ȷ����____________________������ţ���
2NH3(g)+CO2(g)��H=+133.6 kJ/mol�����ڸ÷�Ӧ������˵����ȷ����____________________������ţ���
a���ӷ�Ӧ��ʼ��ƽ��ʱ�����л�������ƽ����Է����������ֲ���
b����ƽ����ϵ������ˮ��������ʹ�÷�Ӧ��ƽ�ⳣ������
c�������¶�ʹ���ص�ת��������
d. ��С�����������ƽ�����淴Ӧ�����ƶ�������ƽ��ʱNH3��Ũ�ȴ���ԭƽ��
��������һ�������¿ɽ����������ﻹԭΪ������
��֪��
�ٽ�Ϣ��е���Ϣ����Ӧ2CO(NH2)2(s)+6NO(g)![]() 5N2(g)+2CO2(g)+4H2O(l)�ġ�H ��_______kJ/mol��
5N2(g)+2CO2(g)+4H2O(l)�ġ�H ��_______kJ/mol��
���ܱ��������Ե����ʵ�����NH3��CO2Ϊԭ�ϣ���120�桢���������·�Ӧ�������أ�CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g)�����������NH3�����ʵ����ٷֺ�����ʱ��仯��ϵ��ͼ��ʾ����a�������Ӧ����v����CO2��______b����淴Ӧ����v����CO2�����>������=����<������������ƽ��ת����Ϊ________________��
CO(NH2)2(s)+H2O(g)�����������NH3�����ʵ����ٷֺ�����ʱ��仯��ϵ��ͼ��ʾ����a�������Ӧ����v����CO2��______b����淴Ӧ����v����CO2�����>������=����<������������ƽ��ת����Ϊ________________��

��2��NO2����Ⱦ����������Na2CO3��Һ����NO2������CO2����֪9.2g NO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol���˷�Ӧ�����ӷ���ʽΪ_________��ǡ�÷�Ӧ��ʹ��Һ�е�CO2��ȫ�ݳ���������Һ�������ԣ�����Һ������Ũ�ȴ�С��ϵ��c(Na��)>______��
��3������ȼ�ϵ��Ϊ��Դ��ͨ�����ӽ���Ĥ��ⷨ���Ƶ��Һ��OH����Ũ�����Ʊ�����Cu2O��װ����ͼ��ʾ��

����װ����B�缫Ӧ���缫__���C����D�������õ����е����ӽ���ĤΪ__������������������ӽ���Ĥ��
���𰸡�a -1804.7kJ/mol > 75% 2NO2+ CO32��=CO2+ NO2��+ NO3�� c��NO3����> c��NO2����> c��OH����>c��H���� D ��
��������
��1���ٻ�ѧƽ�ⳣ����ָ��һ���¶��£����淴Ӧ����ƽ��ʱ���������Ũ��ϵ������֮���뷴Ӧ���Ũ��ϵ������֮���ıȣ����塢��Һ�岻��Ҫ�ڻ�ѧƽ�ⳣ����д����
a�����������ֻ�а�����������̼���������ʵ���֮��Ϊ��ֵ2��1��ƽ����Է����������䣻
b��ƽ�ⳣ��ֻ���¶�Ӱ�죻
c������ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���
d. ��С�����������ƽ��������������������Ӧ�����ƶ���
��������һ�������¿ɽ����������ﻹԭΪ��������Ӧ����ʽΪ��2 CO��NH2��2��s��+6 NO��g��=5 N2��g��+2CO2��g��+4 H2O��l����
��֪����CO(NH2)2 ��s��+H2O��l��![]() 2NH3��g��+CO2��g����H=+133.6kJ/mol��
2NH3��g��+CO2��g����H=+133.6kJ/mol��
��ͼ�ɵ��Ȼ�ѧ����ʽ����4NH3��g��+6 NO��g��=5 N2��g��+6H2O��l����H=-2071.9 kJ/mol��
���ݸ�˹���ɣ�����2+�ڿɵã�2 CO��NH2��2��s��+6 NO��g��=5 N2��g��+2CO2��g��+4 H2O��l����
��a��δ����ƽ�⣬��Ӧ����������Ӧ���У�����Ӧ���ʼ�С���淴Ӧ��������b��ƽ��״̬ʱ����������ȣ�
��NH3��CO2����ʼ���ʵ���Ϊ1mol��ƽ��ʱ����ת����Ϊx����ʾ��ƽ��ʱ��������ʵ�������ϰ������������20%�з��̼��㣻
��2��9.2gNO2�����ʵ���![]() =0.2mol��Na2CO3��Һ��ȫ��Ӧ����CO2ʱת�Ƶ���0.1mol����Ӧ��ֻ��NԪ�ػ��ϼ۱仯����N�Ļ��ϼ۷ֱ���+4�۱仯Ϊ+5�ۺ�+3�ۣ���Ӧ�����ӷ���ʽΪ��2NO2+CO32-=NO3-+NO2-+CO2���ڼ�����Һ��Ӧ����NaNO3��NaNO2������Ũ����ȣ�NO2-ˮ����Һ�ʼ��ԡ�
=0.2mol��Na2CO3��Һ��ȫ��Ӧ����CO2ʱת�Ƶ���0.1mol����Ӧ��ֻ��NԪ�ػ��ϼ۱仯����N�Ļ��ϼ۷ֱ���+4�۱仯Ϊ+5�ۺ�+3�ۣ���Ӧ�����ӷ���ʽΪ��2NO2+CO32-=NO3-+NO2-+CO2���ڼ�����Һ��Ӧ����NaNO3��NaNO2������Ũ����ȣ�NO2-ˮ����Һ�ʼ��ԡ�
��1����a����������ƽ����Է�������= ![]() ����Ӧ��ֻ�������������̼�Ͱ���Ϊ������ʼ�հ����ʵ���֮��Ϊ1��2���ɣ��ʻ�������ƽ����Է�������ʼ�ղ��䣬ѡ��a��ȷ��
����Ӧ��ֻ�������������̼�Ͱ���Ϊ������ʼ�հ����ʵ���֮��Ϊ1��2���ɣ��ʻ�������ƽ����Է�������ʼ�ղ��䣬ѡ��a��ȷ��
b���¶Ȳ��䣬��ѧƽ�ⳣ�����䣬ѡ��b����
c����ӦCO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g)��H=+133.6 kJ/mol����ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ������ص�ת���ʼ�С��ѡ��c����
2NH3(g)+CO2(g)��H=+133.6 kJ/mol����ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ������ص�ת���ʼ�С��ѡ��c����
d. ��С�����������ƽ��������������������Ӧ�����ƶ�������ƽ��ʱ�����������ı�������ƽ���ƶ�����İ��������ı�����NH3��Ũ��С��ԭƽ�⣬ѡ��d����
��ѡa��
��������һ�������¿ɽ����������ﻹԭΪ��������Ӧ����ʽΪ��2 CO��NH2��2��s��+6 NO��g��=5 N2��g��+2CO2��g��+4 H2O��l����
��֪����CO��NH2��2 ��s��+H2O��l��![]() 2NH3��g��+CO2��g����H=+133.6kJ/mol��
2NH3��g��+CO2��g����H=+133.6kJ/mol��
��ͼ�ɵ��Ȼ�ѧ����ʽ����4NH3��g��+6 NO��g��=5 N2��g��+6H2O��l����H=-2071.9 kJ/mol��
���ݸ�˹���ɣ�����2+�ڿɵã�2CO��NH2��2��s��+6NO��g��=5N2��g��+2CO2��g��+4H2O��l����H=-1804.7KJ/mol��
�۰��������������50%�仯Ϊ20%������������ֲ��䣬˵��b�㷴Ӧ�ﵽƽ��״̬��a�㰱������ٷֺ�������b�İ�������ٷֺ�����˵����Ӧ������дﵽƽ��״̬��a�������Ӧ���ʴ���b�������Ӧ���ʣ���v����CO2����v����CO2����
��NH3��CO2����ʼ���ʵ���Ϊ1mol��ƽ��ʱ����ת����Ϊx����
CO2��g��+2NH3��g��![]() CO ��NH2��2 ��s��+H2O��g����
CO ��NH2��2 ��s��+H2O��g����
��ʼ����mol����1 1 0
�仯����mol����0.5x x 0.5x
ƽ������mol����1-0.5x 1-x 0.5x
�������������=![]() =20%�����x=75%��
=20%�����x=75%��
��2��9.2gNO2�����ʵ���![]() =0.2mol��Na2CO3��Һ��ȫ��Ӧ����CO2ʱת�Ƶ���0.1mol����Ӧ��ֻ��NԪ�ػ��ϼ۱仯����N�Ļ��ϼ۷ֱ���+4�۱仯Ϊ+5�ۺ�+3�ۣ���Ӧ�����ӷ���ʽΪ��2NO2+CO32-=NO3-+NO2-+CO2���ڼ�����Һ��Ӧ����NaNO3��NaNO2������Ũ����ȣ�NO2-ˮ����Һ�ʼ��ԣ�������Һ�е�����Ũ�ȴ�С��ϵΪc��Na+����c��NO3-����c��NO2-����c��OH-����c��H+����
=0.2mol��Na2CO3��Һ��ȫ��Ӧ����CO2ʱת�Ƶ���0.1mol����Ӧ��ֻ��NԪ�ػ��ϼ۱仯����N�Ļ��ϼ۷ֱ���+4�۱仯Ϊ+5�ۺ�+3�ۣ���Ӧ�����ӷ���ʽΪ��2NO2+CO32-=NO3-+NO2-+CO2���ڼ�����Һ��Ӧ����NaNO3��NaNO2������Ũ����ȣ�NO2-ˮ����Һ�ʼ��ԣ�������Һ�е�����Ũ�ȴ�С��ϵΪc��Na+����c��NO3-����c��NO2-����c��OH-����c��H+����
��3��ȼ�ϵ������ͨ����������ͨȼ�ϣ���CΪ������DΪ������ͭ�缫�������������ĵ缫����ʽΪ2Cu+2OH--2e-=Cu2O+H2O����ͭΪ��������ԭ��ص�������������B��D��A��C��������ѡB��
�����ܷ�Ӧ����������ӦΪ2Cu+2OH--2e-=Cu2O+H2O���������ӽ���ĤӦ���������ӽ���Ĥ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ﵽ����ʵ��Ŀ�ģ������õķ�����ȷ���ǣ� ��
A. �������ͺ�ˮ�Ļ����������ҺB. ����ˮ�;ƾ��Ļ����������Һ
C. �þƾ��ӵ�ˮ����ȡ��������ȡD. ����ˮ����ȡ��������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����500mL����BaCl2��KCl�Ļ����Һ�ֳ�5�ȷݣ�ȡһ�ݼ��뺬a mol �����Ƶ���Һǡ��ʹ��������ȫ��������ȡһ�ݼ��뺬b mol ����������Һǡ��ʹ��������ȫ��������û����Һ�м�����Ũ��Ϊ�� ��
A. 0.1(b-2a)mol/LB. 10(2a-b)mol/LC. 10(b-a)mol/LD. 10(b-2a)mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ���������ͬ��������Һ����pH=3��CH3COOH��Һ ��pH=3������ ��pH=11�İ�ˮ ��pH=11��NaOH��Һ������˵������ȷ������ ��
A. ����������Һϡ��100����ϡ�ͺ���ҺpH��С˳��>��>��>��
B. ������Ģں͢ۻ������ǿ�������Σ���Ϻ���Һ������
C. ������Ģۺֱܷ͢��õ�Ũ�ȵ�������Һ�кͣ�����������Һ���������>��
D. ������Ģٺ͢ڷֱ���������п����Ӧ���ɵ�������ͬ��ͬѹ���������>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��X��g��+2Y��g��![]() 2Z��g�� ����2M��g��
2Z��g�� ����2M��g��![]() N��g��+P��g���ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܷ���塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ��
N��g��+P��g���ֱ����ܱ�������������Ӧ���н��У���Ӧ��֮������Ħ�����ɻ������ܷ���塣��Ӧ��ʼ�ʹﵽƽ��״̬ʱ�й��������ı仯��ͼ��ʾ��

�����ж���ȷ������ ��
A����Ӧ�ٵ�����Ӧ�����ȷ�Ӧ
B����ƽ����I��ʱ��ϵ��ѹǿ�뷴Ӧ��ʼʱ��ϵ��ѹǿ֮��Ϊ14:15
C����ƽ����I����ƽ����II����M������������
D����ƽ����I��ʱ��X��ת����Ϊ5/11
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ��Ԫ��֮��û�е���ת�Ƶ��ǣ� ��
A.HNO3��NH3��Ӧ����NH4NO3
B.Fe��Cl2�е�ȼ����FeCl3
C.���H2O�Ʊ�H2��O2
D.H2��O2��ȼ�ϵ����ת��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ��(�г���װ��ʡ��)��������ʵ�飬�ܵó���Ӧʵ����۵���
ѡ�� | �� | �� | �� | ʵ����� |
|
A | ϡ���� | Na2S | AgNO3��AgCl����Һ | Ksp(AgCl)>Ksp(Ag2S) | |
B | Ũ���� | ���� | ��ˮ | Ũ���������ˮ�ԡ������� | |
C | ϡ���� | Na2CO3 | CaCl2��Һ | CO2�����Ȼ��Ʒ�Ӧ | |
D | Ũ���� | Na2CO3 | Na2SiO3��Һ | ���ԣ�����>̼��>���� |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CO2��CO��CH4��ɵĻ��������ͬ��ͬѹ���뵪�����ܶ���ͬ����û��������CO2��CH4��CO������ȿ�Ϊ(����)
A.11��4��7B.3��4��1C.4��3��7D.3��2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ø�Ũ�Ⱥ����ˮ(��Ҫ�ɷ�ΪH3AsO3)��ȡAs2O3�Ĺ�����������ͼ��ʾ��
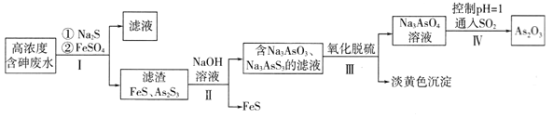
��֪��As2S3(s)+3S2-(aq)![]() 2AsS33-(aq)
2AsS33-(aq)
(1)H3AsO3��AsԪ�صĻ��ϼ�Ϊ______��H3AsO3�ĵ�һ�����뷽��ʽΪ��________��
(2)����I����FeSO4��������______________________��
(3)���������Ӧ�Ļ�ѧ����ʽΪ___________________������III�������������б�������Ԫ����___________(��Ԫ�ط���)��
(4)����IV������Ӧ�����ӷ���ʽΪ________________________��
(5)���÷�ӦAsO43-+2I-+2H+![]() AsO33-+I2+H2O��Ƴ�ԭ��أ���ʼʱ�ڼס��������зֱ����ͼʾҩƷ������װ��(a��b��Ϊʯī�缫)��
AsO33-+I2+H2O��Ƴ�ԭ��أ���ʼʱ�ڼס��������зֱ����ͼʾҩƷ������װ��(a��b��Ϊʯī�缫)��
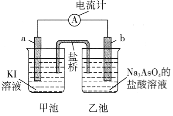
����ʼʱ��b�缫�ĵ缫��ӦʽΪ__________________��
��һ��ʱ��������ָ�벻����ƫת����ʹָ��ƫת��������ʼʱ�෴���ɲ�ȡ�Ĵ�ʩ��______________________________(��һ��)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com