
【题目】下列反应的离子方程式正确的是( )
A.FeCl3溶液腐蚀铜线路板:Fe3++Cu=Fe2++Cu2+
B.氯气通入水中:Cl2+H2O=2H++ClO-+Cl-
C.金属铝加入到NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑
D.Na2O加入稀硫酸中:O2-+2H+=H2O
科目:高中化学 来源: 题型:
【题目】已知铷(![]() )是37号元素,其相对原子质量是85.5,与钠位于同一主族,回答下列问题:
)是37号元素,其相对原子质量是85.5,与钠位于同一主族,回答下列问题:
(1)铷位于第______周期,其原子半径比钠元素的原子半径______(填“大”或“小”)。
(2)铷单质性质活泼,写出在点燃条件下它与氯气反应的化学方程式:________________________;铷单质易与水反应,反应的离子方程式为________________________,实验表明铷与水反应比钠与水反应______(填“剧烈”或“缓慢”);反应过程中铷在水______(填“面”或“底”)与水反应,原因是__________________。
(3)同主族元素的同类化合物的化学性质相似,写出过氧化铷与![]() 反应的化学方程式:________________。
反应的化学方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业甲醇的质量分数可以用下列方法测定:
①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O,反应式为:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72-可用Fe2+与之完全反应:
Cr2O72﹣+ Fe2++ H+- Cr3++ Fe3++ H2O
现有0.12g工业甲醇,在H2SO4溶液中与25mL0.2molL-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1molL-1FeSO4与其反应,结果用去FeSO4溶液9.6mL。
(1)配平第②步中离子方程式___。
(2)计算工业甲醇的质量分数___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状况)气体。回答:

(1)直流电源中,M为________极。
(2)Pt电极上生成的物质是________,其质量为________g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为2∶________∶________∶________。
(4)AgNO3溶液的浓度________(填“增大”“减小”或“不变”,下同),硫酸的浓度________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )

A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO42-)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应Cu+2H2SO4![]() CuSO4+SO2↑+2H2O说法正确的是( )
CuSO4+SO2↑+2H2O说法正确的是( )
A.H2SO4是还原剂B.Cu在反应中被氧化
C.H2SO4在反应中只表现氧化性D.1mol氧化剂在反应中得到1mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫研究。

(1)酸浸时反应的化学方程式为_______。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为:Al2(SO4)x(OH)6-2x。滤渣Ⅱ的主要成分为______(填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是_______(用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是______;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将_______(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NH3是能用来做喷泉实验的气体,若在同温同压下用等体积烧瓶一个收集满NH3,另一个收集NH3和N2的混合气体,如图所示,喷泉实验停止后,两个烧瓶内溶液的关系式(不考虑烧瓶内溶质的扩散,氨水的溶质按NH3计算)( )
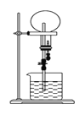
A.溶质的物质的量浓度相同,溶质的质量分数不同
B.溶质的质量分数相同,溶质的物质的量不同
C.溶质的物质的量浓度和溶质的质量分数都不同
D.溶质的物质的量浓度和溶质的质量分数都相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示每一方框表示一种反应物或生成物,其中A、C、D、E、F在通常情况下均为气体,且加热X生成的A与C的物质的量之比为1∶1,B为常见液体。
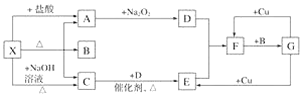
试回答下列问题:
(1)X是________(填化学式,下同),F是__________。
(2)A―→D反应的化学方程式为_______。
(3)G与Cu的反应中,G表现的性质为______。
(4)X与过量NaOH溶液反应生成C的离子方程式为_____________。
(5)以C、B、D为原料可生产G,若使amol C完全转化为G,理论上至少需要D___ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com