
【题目】利用水热和有机溶剂等软化学方法,可合成出含有有机杂化锌、锗以及砷等金属的硒化物,且该硒化物具有离子交换、催化、吸附、半导体等性能,显示出良好的应用前景。回答下列问题:
(1)锌基态原子核外电子排布式为________________。元素锗与砷中,第一电离能较大的是_________(填元素符号,下同),基态原子核外未成对电子数较少的是_______________。
(2)H2SeO3分子中Se原子的杂化形式为____________,H2SeO4的酸性比H2SeO3强,原因是_________。
(3)气态SeO3分子的立体构型为____________,与SeO3互为等电子体的一种离子为_______(填离子符号)。
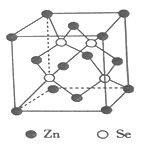
(4)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为____________,若该晶胞密度为ρg·cm-3,硒化锌的摩尔质量为Mg·mol-1。用NA代表阿伏伽德罗常数的数值,则晶胞参数ɑ为____________nm。
【答案】 1s22s22p63s23p63d104s2{[Ar]3d104s2} As Ge sp3 H2SeO4分子中非羟基的氧原子数大于H2SeO3 平面三角形 CO32-(或NO3-) 4 ![]() ×107
×107
【解析】(1)Zn原子核外电子数为30,核外电子排布式为1s22s22p63s23p63d104s2{[Ar]3d104s2};同周期元素从左到右第一电离能逐渐增大,As的4p能级含有3个电子,为半满稳定状态,第一电离能较高,故元素锗与砷中,第一电离能较大的是As;元素锗与砷中,基态原子核外未成对电子数分别为2和3,较少的是Ge;(2) H2SeO3分子中Se原子在S8分子中S原子成键电子对数为4,孤电子对数为1,即价层电子对数为4,所以其杂化轨道类型为sp3;H2SeO3的分子结构为![]() ,Se为+4价,而H2SeO4的分子结构为
,Se为+4价,而H2SeO4的分子结构为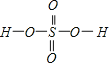 ,Se为+6价,H2SeO4分子中非羟基的氧原子数大于H2SeO3,后者Se原子吸电子能力强,则羟基上氢原子更容易电离出H+;(3)根据价层电子对互斥理论可知,SeO3分子中中心原子含有的孤对电子对数=
,Se为+6价,H2SeO4分子中非羟基的氧原子数大于H2SeO3,后者Se原子吸电子能力强,则羟基上氢原子更容易电离出H+;(3)根据价层电子对互斥理论可知,SeO3分子中中心原子含有的孤对电子对数=![]() =0,即气态SeO3分子中Se形成3个δ键,没有孤电子对,所以该分子形成的空间构型是平面三角形;SeO3是24e-,24e-等电子体有:NO3-、CO32-等;(4)根据硒化锌晶胞结构图可知,每个锌原子周围有4个硒原子,每个硒原子周围也有4个锌原子,所以硒原子的配位数为4,该晶胞中含有硒原子个数为8
=0,即气态SeO3分子中Se形成3个δ键,没有孤电子对,所以该分子形成的空间构型是平面三角形;SeO3是24e-,24e-等电子体有:NO3-、CO32-等;(4)根据硒化锌晶胞结构图可知,每个锌原子周围有4个硒原子,每个硒原子周围也有4个锌原子,所以硒原子的配位数为4,该晶胞中含有硒原子个数为8![]() +6×
+6×![]() =4,根据
=4,根据![]() =
=![]() =
=![]() ,所以V=
,所以V=![]() ,则晶胞的边长为:
,则晶胞的边长为:![]() cm=
cm=![]() ×107nm。
×107nm。


科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.将30 mL 0.5 mol/L NaOH溶液加水稀释到500 mL,所得溶液的NaOH的浓度为0.3 mol/L
B.配制250 mL 1.0 mol/L H2SO4溶液,需要18 mol/L的浓H2SO4的体积约为13.9 mL
C.0.270 kg质量分数为10%的CuCl2溶液中Cl﹣的物质的量为0.2 mol
D.80 g NaOH溶于1 L水中所得的溶液的物质的量浓度为2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.25gmL﹣1 , 质量分数为36.5%的浓盐酸配制240mL 0.1molL﹣1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为 .
(2)配制240mL 0.1molL﹣1的盐酸应量取浓盐酸体积mL,应选用容量瓶的规格mL.
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次) .
A.用30mL水洗涤2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线处
(4)操作A中,将洗涤液都移入容量瓶,其目的是 .
(5)若实验过程中出现如下情况如何处理?
①加蒸馏水时不慎超过了刻度线 .
②向容量瓶中转移溶液时不慎有溶液溅出 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是常用的实验仪器(铁架台和玻璃导管、橡皮管、瓶塞等略去) 
①填写以下仪器的名称:D , J;
②用四氯化碳萃取溴水中Br2单质,萃取能否用酒精代替四氯化碳进行实验? , 解释其原因;
③蒸馏装置中,在E中加入沸石的目的是 , 仪器J的冷凝水应该进出(填写a、b).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四组分散系:①汽油和水形成的乳浊液 ②含有泥沙的食盐水 ③溶有碘(I2)的碘化钾溶液 ④乙二醇和丙三醇混合溶液(乙二醇和丙三醇的部分物理性质见下表).
物质 | 熔点/℃ | 沸点/℃ | 密度/gcm﹣3 | 溶解性 |
乙二醇 | ﹣11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
请用下图所示的仪器分离以上各混合液,仪器和方法不能对应的是( )
A.①﹣(3)﹣分液
B.②﹣(2)﹣过滤
C.③﹣(2)﹣萃取
D.④﹣(1)﹣蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我们主要从三个方面讨论一个化学反应的原理,其中不属于这三个方面的是
A.反应进行的方向B.反应的快慢C.反应进行的限度D.反应物或生成物的颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作或测量数据的说法正确的是( )
A.用托盘天平称量食盐的质量为12.35gB.中和热的测定实验中,NaOH溶液应该稍过量
C.用pH试纸测量次氯酸钠溶液的pH为11D.用碱式滴定管量取高锰酸钾溶液20.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)===C(g) ΔH,分两步进行:
①A(g)+B(g)===X(g) ΔH1
②X(g)===C(g) ΔH2
反应过程中能量变化如下图所示,E1表示A+B===X的活化能,下列说法正确的是
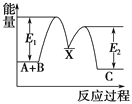
A. ΔH1=ΔH-ΔH2>0
B. X是反应A(g)+B(g)===C(g)的催化剂
C. E2是反应②的反应热
D. ΔH=E1-E2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:实验室可供选择的用于去除气体杂质的试剂有:浓硫酸、无水氯化钙、五氧化二磷、碱石灰(主要成分为NaOH和CaO) 
①实验室用如图1所示装置进行纯净干燥的氢气还原氧化铁实验.a装置名称为 , 方框B内应选用如图2装置(填“Ⅰ”或“Ⅱ”),选用的除杂试剂为(填试剂名称).
②实验室常用36.5%浓盐酸(ρ=1.2gcm﹣3)配制稀盐酸,若要配制500mL,0.5molL﹣1稀盐酸,需用量筒取用浓盐酸mL.
③写出装置C中发生反应的化学方程式并用单线桥标明电子的转移 . 实验结束时应该采取的操作是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com