
【题目】一定温度下水溶液中H+ 和OH- 的浓度变化曲线如图,下列说法正确的是
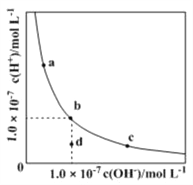
A. 升高温度,可能引起c向b的变化
B. 该温度下,水的离子积常数为![]()
C. 该温度下,加入HCl可能引起由b向a的变化
D. 该温度下,稀释溶液可能引起由c向d的变化
科目:高中化学 来源: 题型:
【题目】以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )
氧化物 | 环境问题 | 主要来源 | |
A | CO2 | 酸雨 | 化石燃料的燃烧 |
B | CO | CO中毒 | 汽车尾气和化石燃料的不完全燃烧 |
C | NO2 | 温室效应 | 工厂废气的排放 |
D | SO2 | 光化学烟雾 | 汽车尾气的排放 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4、CO2和碳酸都是碳的重要化合物,实现碳及其化合物的相互转化,对开发新能源和降低碳排放意义重大。
(1)已知:①CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.1kJmol—1
CO(g)+3H2(g) △H1=+206.1kJmol—1
②2H2(g)+CO(g)![]() CH3OH(l) △H2=-128.3kJmol—1
CH3OH(l) △H2=-128.3kJmol—1
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJmol—1
写出由甲烷和氧气合成液态甲醇的热化学方程式:_____________________。
(2)若利用反应①来制备氢气。为了探究温度、压强对反应①的影响,设计以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa)。
实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/ mol·L—1 | H2O初始浓度/ mol·L—1 |
1 | 400 | 101 | 3.0 | 7.0 |
2 | T | 101 | 3.0 | 7.0 |
3 | 400 | P | 3.0 | 7.0 |
Ⅰ、实验1、实验2和实验3比较,反应开始时正反应速率最快的是_________;平衡时CH4的转化率最小的是_________。
Ⅱ、实验2和实验3相比,其平衡常数关系:K2______K3(填“>”、“<”或“=”)。
(3)科学家提出由CO2制取碳(C)的太阳能工艺如图1所示.
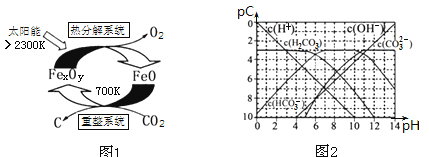
①“重整系统”发生的反应中n(FeO)∶n(CO2)=6∶1,则FexOy的化学式为______;
②“热分解系统”中每分解l mol FexOy,同时生成标准状况下气体体积为_______。
(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值。如某溶液中溶质的浓度为1×10—2molL—1,则该溶液中溶质的pC=﹣lg(1×10—2)=2。上图2为25℃时H2CO3溶液的pC﹣pH图。请回答下列问题:
①
②在8<pH<10时,溶液中HCO3—的pC值不随着pH增大而减小的原因是____;
③求H2CO3一级电离平衡常数的数值Ka1= _______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,一密闭容器被无摩擦、可滑动的两隔板A、B分成甲、乙两室。标准状况下,在乙室充入8.4g N2,甲室充入8.8g H2和O2的混合气体。
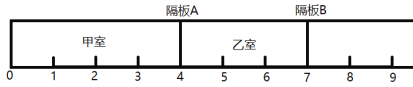
(1)甲室中H2与O2的质量比为_____________,甲室中原子个数约为 ____________个。
(2)维持温度不变,将隔板A固定在“3”处,将隔板B固定在“5”处,此时甲、乙两室中气体的压强比P(甲):P(乙)=______________。
(3)用电火花处理甲室中的气体使其充分反应,反应后恢复至标准状况。甲室与乙室此时的体积比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,醋酸和氨水的电离常数均为1.8×10-5。现取浓度均为0.1mol/L的醋酸溶液与氨水各20mL,分别用0.1mol/L的NaOH溶液、0.1mol/L盐酸进行中和滴定,滴定过程中pH滴加溶液的体积变化关系如图所示。下列说法正确的是
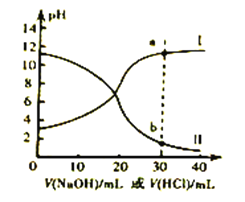
A. 曲线I中,滴加溶液到10mL时:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-)
B. 曲线II中,滴加溶液到20mL时: c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. 曲线II中,滴加溶液时始终存在: c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
D. 若将a和b两点对应的溶液混合,所得溶液常温下pH<7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,pH=2的两种一元酸HX、HY各取5 mL,分别加水稀释,溶液pH变化与所加水的体积关系如图所示(忽略混合溶液体积的变化),下列说法错误的是
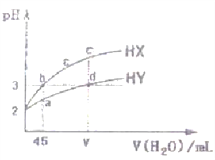
A. 分别取等体积a、b两点溶液,完全中和需同浓度NaOH溶液的体积V(HX)=V(HY)
B. b、d两点溶液中由水电离产生的H+浓度![]()
C. 相同条件下,a、b、c、d、e五点溶液的导电性大小顺序为:a>b=d>c>e
D. 加入NaOH溶液,可以使d点c(Y-)增大、c(H+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“1998年中国十大科技成果”之一是合成一维纳米氮化镓。已知氮化镓中镓是第ⅢA族元素,则氮化镓的化学式可能为( )
A.GaNB.Ga2N3C.Ga3N2D.GaN2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2CO3溶液可制得NaHCO3和NaOH,原理如图所示。
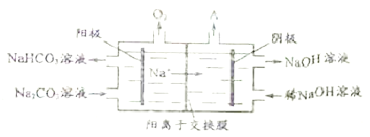
(1)阳极生成HCO3- 的电极反应式为________________________________,阴极产生的物质A的化学式为______________;
(2)工作一段时间后,两极区制得NaHCO3与NaOH的物质的量之比约为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com