
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的部分生成物和反应的条件没有标出)。
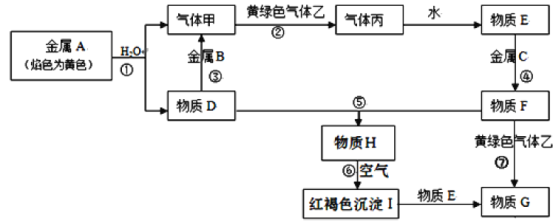
请回答下列问题:
【1】D、F、G的化学式分别是
A.NaOH、FeCl2、FeCl3B.NaOH、FeCl3、FeCl2
C.Fe3O4、FeCl2、FeCl3D.Fe3O4、FeCl3、FeCl2
【2】A、B、C的金属活动性顺序是
A.A>B>CB.A>C>BC.B>A>CD.C>B>A
【3】①~⑦反应中未涉及到四种基本反应类型中的
A.化合反应B.分解反应C.置换反应D.复分解反应
【4】除去F溶液中的少量G,常加入或通入足量的。
A.铁粉B.氯气C.双氧水D.酸性高锰酸钾溶液
【5】除去乙中的少量丙,常将混合气通入到中进行洗气。
A.NaOH溶液B.饱和食盐水C.饱和NaHCO3溶液D.浓硫酸
【答案】
【1】A
【2】A
【3】B
【4】A
【5】B
【解析】
金属单质A焰色反应为黄色,则A为Na,钠与水反应生成气体甲为H2,D为NaOH,金属单质B和氢氧化钠溶液反应生成氢气,则B为Al,黄绿色气体乙为Cl2,乙与H2反应生成气体丙为HCl,HCl溶于水得到E为盐酸,金属单质C与盐酸反应得到F,F与物质D(氢氧化钠)反应生成H,H在空气中转化为红褐色沉淀I,则H为Fe(OH)2,红褐色沉淀I为Fe(OH)3,所以金属C为Fe,则F为FeCl2,FeCl2与Cl2反应产生的物质G为FeCl3。然后根据各个小题的问题逐一解答。
【1】根据上述分析可知:D是NaOH,F是FeCl2,G是FeCl3,所以合理选项是A。
【2】A是Na,B是Al,C是Fe,根据金属在金属活动性顺序表中的位置可知三种金属的活动性有强到弱的顺序为:A>B>C,故合理选项是A。
【3】①是Na与H2O发生置换反应产生NaOH和H2;②是H2与Cl2发生化合反应产生HCl;③是Al与NaOH溶液反应产生NaAlO2和H2,反应不属于任何一种基本类型;④是Fe与HCl发生置换反应产生FeCl2和H2;⑤是NaOH与FeCl2发生复分解反应产生Fe(OH)2和NaCl;⑥是Fe(OH)2、O2、H2O发生化合反应产生Fe(OH)3;⑦是FeCl2和Cl2发生化合反应产生FeCl3。可见,在上述反应中未涉及的基本反应类型为分解反应,故合理选项是B。
【4】F为FeCl2, G为FeCl3,除去FeCl2中少量杂质FeCl3,可根据FeCl3的氧化性,及不能引入新的杂质的要求,向溶液中加入足量Fe粉,发生反应:Fe+2FeCl2=3FeCl3,然后过滤除去固体物质,就得到纯净的FeCl2溶液,故合理选项是A。
【5】乙是Cl2,丙是HCl,要除去Cl2中的少量HCl,可根据Cl2与水产生HCl、HClO的反应是可逆反应的特点,及HCl极容易溶于水,利用平衡移动原理,将混合气通入到饱和NaCl溶液中进行洗气,故合理选项是B。
本题考查无机物推断,涉及Na、Al、Fe元素单质及化合物性质和Cl2的性质,A的焰色反应、I的颜色是推断突破口,需要学生熟练掌握元素化合物性质及物质反应类型。


科目:高中化学 来源: 题型:
【题目】下列离子组在给定条件下离子共存判断及反应的离子方程式均正确的是( )
选项 | 条件 | 离子组 | 离子共存判断及反应的离子方程式 |
A | 滴加氨水 | Na+、Al3+、Cl-、NO3- | 不能大量共存,Al3++3OH-=Al(OH)3↓ |
B | 由水电离出的H+浓度为1×10-12molL-1 |
| 一定能大量共存
|
C | pH=1的溶液 | Fe2+、Al3+、 | 不能大量共存,5Fe2++ |
D | 通入少量SO2气体 | K+、Na+、ClO-、 | 不能大量共存,2ClO-+SO2+H2O=2HClO+ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假设12C的相对原子质量为24,如果以0.024 kg12C所含的原子数为阿伏加德罗常数,下列数值中肯定不变的是( )
A.氢气的摩尔质量
B.16 g氧气所含的分子数
C.氧气的相对分子质量
D.一定条件下,跟2 g氢气相化合的氧气的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.9 g 镁铝合金投入到足量的NaOH溶液中,共产生标准状况下H2的体积为3.36 L。则原合金中镁和铝的物质的量之比是
A.1:1B.1:2C.1:3D.2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一新型、高效、无毒的多功能水处理剂。
(资料)K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4。
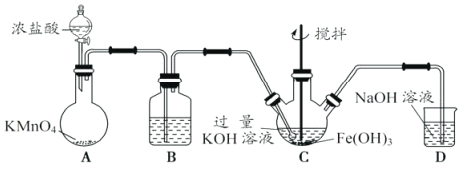
①A为制取氯气发生装置,其中盛放浓盐酸的仪器名称为___________。
②除杂装置B中的试剂为___________。
③C为制备K2FeO4装置,KOH溶液过量的原因是___________。
④D为尾气处理装置,发生反应的离子方程式为___________。
(2)探究 K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黃绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案I中溶液变红可知a中含有___________。该离子的产生___________(填“能”或“不能”)判断一定是由K2FeO4被Cl-还原而形成的。
②方案Ⅱ用KOH溶液洗涤的目的是___________。方案Ⅱ得出氧化性:Cl2___________FeO42-(填“>”或“<”)
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:_______ FeO42-+______H+===_______O2↑+________Fe3++________(配平及完成上述离子方程式)________。现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为___________。(计算结果保留到0.1%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推法在化学学习中经常采用,下列类推的结论正确的是( )
A.Cl2+2KBr= 2KCl+Br2,所以F2也能与KBr溶液反应置换出Br2
B.常温下,Cu+4HNO3(浓)= Cu(NO3)2+2NO2↑+2H2O,所以Fe也能与浓硝酸反应产生NO2
C.Cu+Cl2![]() CuCl2,所以Cu+I2
CuCl2,所以Cu+I2![]() CuI2
CuI2
D.钾保存在煤油中,所以钠也可以保存在煤油中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组制备氯气并对产生氯气的条件进行探究。

(1)装置A中用MnO2与浓盐酸反应制取Cl2,利用了浓HCl的___________(填“氧化性”或“还原性”)。
(2)A中产生的气体不纯,含有的杂质可能是___________。
(3)B用于收集Cl2,请完善装置B并用箭头标明进出气体方向_____________。
(4)C用于吸收多余的Cl2,C中发生反应的离子方程式是____________________________________________________________。
(5)该小组欲研究盐酸的浓度对制Cl2的影响,设计实验进行如下探究。

①已知MnO2呈弱碱性。 Ⅰ中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是___________________________________________________。
②Ⅱ中发生了分解反应,反应的化学方程式是__________________________________。
③Ⅲ中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验Ⅳ进行探究:

将实验Ⅲ、Ⅳ作对比,得出的结论是____________________________;
将ⅰ、ⅱ作对比,得出的结论是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列说法正确的是
A.28g的CO与CO2混合物中含有的碳原子数为NA
B.标准状况下,22.4 L水中含有的氧原子数为NA
C.0.5molL﹣1的AlCl3溶液中所含Cl- 数目为1.5NA
D.1mol钠在足量氧气中燃烧生成Na2O2,转移的电子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com