
碘单质难溶于水却易溶于KI溶液。碘水中加入KI溶液发生反应:I2(aq)+I-(aq) I3—(aq),该反应的平衡常数与温度的关系如图,下列说法不正确的是( )
I3—(aq),该反应的平衡常数与温度的关系如图,下列说法不正确的是( )
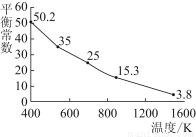
A.上述正反应为放热反应
B.上述体系中加入苯,平衡不移动
C.可运用该反应原理除去硫粉中少量的碘单质
D.实验室配制碘水时,为增大碘单质的溶解度可加入适量KI溶液
科目:高中化学 来源:2014高考化学名师知识点精编 专题10盐类水解与沉淀溶解平衡练习卷(解析版) 题型:选择题
一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm-),称为难溶电解质的溶度积。已知下表数据:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp/25 ℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | ≥3 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的下列说法,正确的是( )
A.向该混合溶液中逐滴加入NaOH溶液,最先看到的是蓝色沉淀
B.该溶液中c(S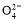 )∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
)∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
C.向该溶液中加入适量氯水,调节pH到4~5后过滤,可获得纯净的CuSO4溶液
D.向该溶液中加入适量氨水,调节pH到9.6后过滤,将所得沉淀灼烧,可得等物质的量的CuO、FeO、Fe2O3三种固体的混合物
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题8电解质溶液练习卷B(解析版) 题型:选择题
25 ℃时,关于浓度均为0.2 mol/L的Na2CO3和NaHCO3溶液的说法不正确的是( )
A.两溶液中均存在电离平衡和水解平衡
B.两溶液分别加水稀释后,pH和KW均减小
C.两溶液中均存在c(OH-)+2c(CO32—)+c(HCO3—)=c(Na+)+c(H+)
D.c(OH-)前者大于后者
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题8电解质溶液练习卷A(解析版) 题型:选择题
25 ℃时,浓度均为0.1 mol·L-1的HA溶液和BOH溶液,pH分别是1和11。下列说法正确的是( )
A.在0.1 mol·L-1BA溶液中,c(A-)+c(H+)=c(BOH)+c(B+)
B.若将0.1 mol·L-1 BOH溶液稀释至0.001 mol·L-1则溶液的pH=9
C.若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+)
D.若将上述两溶液按体积比1∶1混合,则混合液中:c(A-)>c(B+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题7化学反应速率和化学平衡练习卷B(解析版) 题型:选择题
含Cd2+废水可通过如下反应转化为CdS,以消除镉对环境的污染:
Cd2+(aq)+H2S(g) CdS(s)+2H+(aq) ΔH<0
CdS(s)+2H+(aq) ΔH<0
该反应达到平衡后,改变横坐标表示的条件,下列示意图正确的是( )
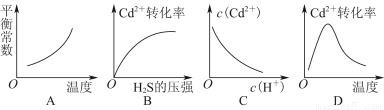
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题7化学反应速率和化学平衡练习卷A(解析版) 题型:选择题
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.2 kJ·mol-1,测得0到10 s内,c(H2)减小了0.75 mol·L-1,下列说法正确的是( )
2NH3(g) ΔH=-92.2 kJ·mol-1,测得0到10 s内,c(H2)减小了0.75 mol·L-1,下列说法正确的是( )
A.10 s到15 s内c(NH3)增加量等于0.25 mol·L-1
B.10 s内氨气的平均反应速率为0.025 mol·L-1·s-1
C.达平衡后,分离出少量NH3,v正增大
D.该反应的逆反应的活化能不小于92.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题6物质结构与元素周期律练习卷(解析版) 题型:选择题
甲、乙、丙、丁是原子序数依次增大的4种短周期元素,A、B、C、D、E是由其中的2种或3种元素组成的化合物,F是由丙元素形成的单质。已知:A+B=D+F,A+C=E+F; 0.1 mol·L-1D溶液的pH为13(25 ℃)。下列说法正确的是( )
A.原子半径:丁>丙>乙>甲
B.乙元素在周期表中的位置为第三周期第ⅣA族
C.1 mol A与足量B完全反应共转移了1 mol电子
D.1.0 L 0.1 mol·L-1E溶液中阴离子总的物质的量小于0.1 mol
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题5化学反应中的能量变化练习卷(解析版) 题型:选择题
反应A(g)+B(g)―→C(g) ΔH,分两步进行:①A(g)+B(g)―→X(g) ΔH1;②X(g)―→C(g) ΔH2。反应过程中能量变化如图1所示,E1表示A+B―→X的活化能,下列说法正确的是( )
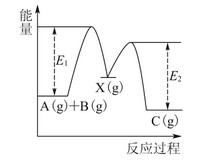
A.ΔH1=ΔH-ΔH2>0
B.X是反应A(g)+B(g)―→C(g)的催化剂
C.E2是反应②的活化能
D.ΔH=E1-E2
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题15化学与技术练习卷(解析版) 题型:填空题
银氨溶液放久后会产生叠氮化银(AgN3)而引起爆炸,直接排放会污染环境,且造成银资源的浪费。某研究小组设计了从银镜反应后的废液中(含过量的银氨溶液,假设不含单质银)回收银的如下两种实验流程:
(已知:[Ag(NH3)2]+在溶液中存在平衡:[Ag(NH3)2]+??Ag++2NH3)
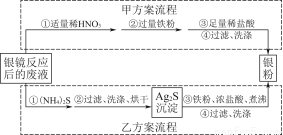
(1)写出甲方案第①步废液与稀HNO3反应的离子方程式 。
(2)甲方案第②步加入的铁粉要过量的目的是 。
甲方案流程可能产生的大气污染物是 。
(3)乙方案若最终得到银粉的质量偏大,排除未洗涤干净的因素,可能的原因是 。
(4)实验室配制银氨溶液的操作过程是 。
(5)已知乙方案第③步反应有H2S气体产生,若最终得到银粉21.6 g,不考虑其他损失,理论上该步需要加入铁粉 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com